ბუნებრივი ცილები. ბუნებრივი ცილების თვისებები
პროტეინები ან ცილები არის რთული, მაღალმოლეკულური ორგანული ნაერთები, რომლებიც შედგება ამინომჟავებისგან. ისინი წარმოადგენენ ცხოველური და მცენარეული ორგანიზმების ყველა უჯრედისა და ქსოვილის ძირითად, ყველაზე მნიშვნელოვან ნაწილს, რომლის გარეშეც სასიცოცხლო ფიზიოლოგიური პროცესები ვერ განხორციელდება. ცილები განსხვავებულია მათი შემადგენლობითა და თვისებებით სხვადასხვა ცხოველურ და მცენარეულ ორგანიზმებში და ერთი და იმავე ორგანიზმის სხვადასხვა უჯრედებსა და ქსოვილებში. სხვადასხვა მოლეკულური შემადგენლობის ცილები განსხვავებულად იხსნება მარილის წყალხსნარებში და არ იხსნება ორგანულ გამხსნელებში. ცილის მოლეკულაში მჟავე და ძირითადი ჯგუფების არსებობის გამო, მას აქვს ნეიტრალური რეაქცია.
ცილები ქმნიან უამრავ ნაერთს ნებისმიერ ქიმიურ ნივთიერებასთან, რაც განსაზღვრავს მათ განსაკუთრებულ მნიშვნელობას ორგანიზმში მიმდინარე ქიმიურ რეაქციებში და წარმოადგენს სიცოცხლის ყველა გამოვლინების საფუძველს და მის დაცვას მავნე ზემოქმედებისგან. ცილები ქმნიან ფერმენტების, ანტისხეულების, ჰემოგლობინის, მიოგლობინის, მრავალი ჰორმონის საფუძველს და ქმნიან ვიტამინებთან კომპლექსურ კომპლექსებს.
ცხიმებთან და ნახშირწყლებთან შერწყმით, ცილები შეიძლება გარდაიქმნას ცხიმებად და ნახშირწყლებად ორგანიზმში მათი დაშლის დროს. ცხოველის ორგანიზმში ისინი სინთეზირდება მხოლოდ ამინომჟავებისა და მათი კომპლექსებისგან - პოლიპეპტიდებისგან და ისინი ვერ წარმოიქმნება არაორგანული ნაერთებისგან, ცხიმებისა და ნახშირწყლებისგან. ბევრი დაბალმოლეკულური ბიოლოგიურად აქტიური ცილოვანი ნივთიერება, რომელიც სხეულშია ნაპოვნი, როგორიცაა ზოგიერთი ჰორმონი, სინთეზირდება სხეულის გარეთ.
ზოგადი ინფორმაცია ცილების და მათი კლასიფიკაციის შესახებ
ცილები ყველაზე მნიშვნელოვანი ბიოორგანული ნაერთებია, რომლებიც ნუკლეინის მჟავებთან ერთად განსაკუთრებულ როლს ასრულებენ ცოცხალ მატერიაში - ამ ნაერთების გარეშე სიცოცხლე შეუძლებელია, რადგან ფ. ენგელსის განმარტებით სიცოცხლე არის ცილოვანი სხეულების განსაკუთრებული არსებობა და ა.შ. .
ცილები არის ბუნებრივი ბიოპოლიმერები, რომლებიც წარმოადგენენ ბუნებრივი ალფა ამინომჟავების პოლიკონდენსაციის რეაქციის პროდუქტებს.
არსებობს 18-23 ბუნებრივი ალფა ამინომჟავა, მათი კომბინაცია ქმნის ცილის მოლეკულების უსასრულოდ დიდ რაოდენობას, რაც უზრუნველყოფს სხვადასხვა ორგანიზმების მრავალფეროვნებას. მოცემული სახეობის ცალკეულ ორგანიზმებსაც კი ახასიათებთ საკუთარი პროტეინები და მრავალი ცილა გვხვდება ბევრ ორგანიზმში.
პროტეინებს ახასიათებთ შემდეგი ელემენტარული შემადგენლობა: მათ წარმოქმნიან ნახშირბადი, წყალბადი, ჟანგბადი, აზოტი, გოგირდი და ზოგიერთი სხვა ქიმიური ელემენტი. ცილის მოლეკულების მთავარი მახასიათებელია მათში აზოტის სავალდებულო არსებობა (გარდა C, H, O ატომებისა).
ცილის მოლეკულებში რეალიზდება "პეპტიდური" ბმა, ანუ კავშირი კარბონილის ჯგუფის C ატომსა და ამინო ჯგუფის აზოტის ატომს შორის, რაც განსაზღვრავს ცილის მოლეკულების ზოგიერთ მახასიათებელს. ცილის მოლეკულის გვერდითი ჯაჭვები შეიცავს უამრავ რადიკალებს და ფუნქციურ ჯგუფებს, რაც "აქცევს" ცილის მოლეკულას მრავალფუნქციურს, რომელსაც შეუძლია მრავალი ფიზიკურ-ქიმიური და ბიოქიმიური თვისებები.
ცილის მოლეკულების მრავალფეროვნებისა და მათი შემადგენლობისა და თვისებების სირთულის გამო, ცილებს აქვთ რამდენიმე განსხვავებული კლასიფიკაცია სხვადასხვა მახასიათებლებზე დაყრდნობით. მოდით შევხედოთ ზოგიერთ მათგანს.
I. მათი შემადგენლობის მიხედვით განასხვავებენ ცილების ორ ჯგუფს:
1. პროტეინები (მარტივი ცილები; მათ მოლეკულას წარმოქმნის მხოლოდ ცილა, მაგალითად კვერცხის ალბუმინი).
2. პროტეიდები რთული ცილებია, რომელთა მოლეკულები შედგება ცილოვანი და არაცილოვანი კომპონენტებისგან.
პროტეიდები იყოფა რამდენიმე ჯგუფად, რომელთაგან ყველაზე მნიშვნელოვანია:
1) გლიკოპროტეინები (ცილისა და ნახშირწყლების რთული კომბინაცია);
2) ლიპოპროტეინები (ცილის მოლეკულების და ცხიმების (ლიპიდების) კომპლექსი;
3) ნუკლეოპროტეინები (ცილის მოლეკულების და ნუკლეინის მჟავის მოლეკულების კომპლექსი).
II. მოლეკულის ფორმის მიხედვით განასხვავებენ ცილების ორ ჯგუფს:
1. გლობულური ცილები - ცილის მოლეკულას აქვს სფერული ფორმა (გლობულის ფორმა), მაგალითად, კვერცხის ალბუმინის მოლეკულები; ასეთი ცილები ან წყალში ხსნადია ან შეუძლიათ კოლოიდური ხსნარების წარმოქმნა.
2. ბოჭკოვანი ცილები - ამ ნივთიერებების მოლეკულებს აქვთ ძაფების (ფიბრილების) ფორმა, მაგალითად, კუნთების მიოზინი, აბრეშუმის ფიბროინი. ფიბრილარული ცილები წყალში უხსნადია, ისინი ქმნიან სტრუქტურებს, რომლებიც ახორციელებენ კონტრაქტურ, მექანიკურ, ფორმის ფორმირებას და დამცავ ფუნქციებს, აგრეთვე სხეულის უნარს გადაადგილდეს სივრცეში.
III. სხვადასხვა გამხსნელებში მათი ხსნადობის მიხედვით ცილები იყოფა რამდენიმე ჯგუფად, რომელთაგან ყველაზე მნიშვნელოვანია შემდეგი:
1. წყალში ხსნადი.
2. ცხიმში ხსნადი.
არსებობს ცილების სხვა კლასიფიკაცია.
ბუნებრივი ალფა ამინომჟავების მოკლე მახასიათებლები
ბუნებრივი ალფა ამინომჟავები არის ამინომჟავის ტიპი. ამინომჟავა არის მრავალფუნქციური ორგანული ნივთიერება, რომელიც შეიცავს მინიმუმ ორ ფუნქციურ ჯგუფს - ამინოჯგუფს (-NH 2) და კარბოქსილის (კარბოქსილის, ეს უკანასკნელი უფრო სწორია) ჯგუფს (-COOH).
ალფა ამინომჟავები არის ამინომჟავები, რომლებშიც ამინო და კარბოქსილის ჯგუფები განლაგებულია იმავე ნახშირბადის ატომზე. მათი ზოგადი ფორმულაა NH 2 CH(R)COOH. ქვემოთ მოცემულია ზოგიერთი ბუნებრივი ალფა ამინომჟავის ფორმულები; ისინი იწერება პოლიკონდენსაციის რეაქციის განტოლებების დასაწერად ხელსაყრელ ფორმაში და გამოიყენება, როდესაც აუცილებელია რეაქციის განტოლებების (სქემების) დაწერა გარკვეული პოლიპეპტიდების წარმოებისთვის:
1) გლიცინი (ამინოძმარმჟავა) - MH 2 CH 2 COOH;
2) ალანინი - NH 2 CH (CH 3) COOH;
3) ფენილალანინი - NH 2 CH (CH 2 C 6 H 5) COOH;
4) სერინი - NH 2 CH(CH 2 OH)COOH;
5) ასპარტინის მჟავა - NH 2 CH (CH 2 COOH) COOH;
6) ცისტეინი - NH 2 CH (CH 2 SH) COOH და ა.შ.
ზოგიერთი ბუნებრივი ალფა ამინომჟავა შეიცავს ორ ამინო ჯგუფს (მაგალითად, ლიზინს), ორ კარბოქსი ჯგუფს (მაგალითად, ასპარტინის და გლუტამინის მჟავები), ჰიდროქსიდის (OH) ჯგუფს (მაგალითად, ტიროზინი) და შეიძლება იყოს ციკლური (მაგალითად, პროლინი). ).
ბუნებრივი ალფა ამინომჟავების მეტაბოლიზმზე გავლენის ბუნებიდან გამომდინარე, ისინი იყოფა ჩანაცვლებად და შეუცვლელებად. აუცილებელი ამინომჟავები ორგანიზმს საკვებით უნდა მიეწოდოს.
ცილის მოლეკულების სტრუქტურის მოკლე აღწერა
გარდა რთული შემადგენლობისა, ცილებს ახასიათებთ ცილის მოლეკულების რთული აგებულებაც. ცილის მოლეკულების ოთხი ტიპის სტრუქტურა არსებობს.
1. პირველადი სტრუქტურა ხასიათდება პოლიპეპტიდურ ჯაჭვში ალფა ამინომჟავების ნარჩენების განლაგების თანმიმდევრობით. მაგალითად, ტეტრაპეპტიდი (პოლიპეპტიდი, რომელიც წარმოიქმნება ოთხი ამინომჟავის მოლეკულის პოლიკონდენსაციის შედეგად) ალა-ფენ-ტირო-სერინი არის ალანინის, ფენილალანინის, ტიროზინის და სერინის ნარჩენების თანმიმდევრობა, რომლებიც დაკავშირებულია ერთმანეთთან პეპტიდური ბმით.
2. ცილის მოლეკულის მეორადი სტრუქტურა არის პოლიპეპტიდური ჯაჭვის სივრცითი განლაგება. ეს შეიძლება იყოს განსხვავებული, მაგრამ ყველაზე გავრცელებული არის ალფა სპირალი, რომელსაც ახასიათებს სპირალის გარკვეული „ნაბიჯი“, ზომა და მანძილი სპირალის ცალკეულ მოხვევებს შორის.
ცილის მოლეკულის მეორადი სტრუქტურის სტაბილურობა უზრუნველყოფილია სპირალის ცალკეულ მოხვევებს შორის სხვადასხვა ქიმიური ბმების წარმოქმნით. მათ შორის ყველაზე მნიშვნელოვანი როლი ეკუთვნის წყალბადურ კავშირს (განხორციელებული ჯგუფების ატომის ბირთვის შეყვანით - NH 2 ან =NH ჟანგბადის ან აზოტის ატომების ელექტრონულ გარსში), იონურ კავშირს (განხორციელებული -COO-ს ელექტროსტატიკური ურთიერთქმედებით. - და - NH + 3 ან =NH იონები + 2) და სხვა სახის კომუნიკაცია.
3. ცილის მოლეკულების მესამეული სტრუქტურა ხასიათდება ალფა სპირალის ან სხვა სტრუქტურის სივრცითი განლაგებით. ასეთი სტრუქტურების სტაბილურობა განისაზღვრება იმავე ტიპის კავშირებით, როგორც მეორადი სტრუქტურა. მესამეული სტრუქტურის განხორციელების შედეგად წარმოიქმნება ცილის მოლეკულის „ქვეერთეული“, რომელიც დამახასიათებელია ძალიან რთული მოლეკულებისთვის, ხოლო შედარებით მარტივი მოლეკულებისთვის მესამეული სტრუქტურა საბოლოოა.
4. ცილის მოლეკულის მეოთხეული სტრუქტურა არის ცილის მოლეკულების ქვედანაყოფების სივრცითი განლაგება. დამახასიათებელია რთული ცილების, როგორიცაა ჰემოგლობინი.
ცილის მოლეკულების სტრუქტურის განხილვისას აუცილებელია განვასხვავოთ ცოცხალი ცილის სტრუქტურა - მშობლიური სტრუქტურა და მკვდარი ცილის სტრუქტურა. ცოცხალ მატერიაში ცილა (მშობლიური ცილა) განსხვავდება ცილისგან, რომელიც ექვემდებარება ცვლილებას, რომლის დროსაც მან შეიძლება დაკარგოს ცოცხალი ცილის თვისებები. ზედაპირულ ექსპოზიციას ეწოდება დენატურაცია, რომლის დროსაც შესაძლებელია ცოცხალი ცილის თვისებების შემდგომი აღდგენა. დენატურაციის ერთ-ერთი სახეობაა შექცევადი კოაგულაცია. შეუქცევადი კოაგულაციის დროს, მშობლიური ცილა იქცევა "მკვდარ ცილად".
ცილის ფიზიკური, ფიზიკოქიმიური და ქიმიური თვისებების მოკლე აღწერა
ცილის მოლეკულების თვისებებს დიდი მნიშვნელობა აქვს მათი ბიოლოგიური და გარემო თვისებების რეალიზაციისთვის. ამრიგად, მათი აგრეგაციის მდგომარეობის მიხედვით, ცილები კლასიფიცირდება როგორც მყარი ნივთიერებები, რომლებიც შეიძლება იყოს ხსნადი ან უხსნადი წყალში ან სხვა გამხსნელებში. ცილების ბიოეკოლოგიური როლის დიდი ნაწილი განისაზღვრება ფიზიკური თვისებებით. ამრიგად, ცილის მოლეკულების უნარი შექმნან კოლოიდური სისტემები განსაზღვრავს მათ კონსტრუქციულ, კატალიზურ და სხვა ფუნქციებს. ცილების წყალში და სხვა გამხსნელებში უხსნადობა, მათი ფიბრილარულობა განაპირობებს დამცავ და ფორმის ფორმირების ფუნქციებს და ა.შ.
ცილების ფიზიკურ-ქიმიური თვისებები მოიცავს მათ დენატურაციისა და კოაგულაციის უნარს. კოაგულაცია ვლინდება კოლოიდურ სისტემებში, რომლებიც ნებისმიერი ცოცხალი ნივთიერების საფუძველია. კოაგულაციის დროს ნაწილაკები უფრო დიდი ხდება მათი ერთმანეთთან შეკვრის გამო. კოაგულაცია შეიძლება იყოს დამალული (მისი დაკვირვება მხოლოდ მიკროსკოპით) და აშკარა - მისი ნიშანი ცილის ნალექია. კოაგულაცია შეუქცევადია, როდესაც კოაგულაციის ფაქტორის მოქმედების შეწყვეტის შემდეგ კოლოიდური სისტემის სტრუქტურა არ აღდგება და შექცევადია, როდესაც კოაგულაციის ფაქტორის მოხსნის შემდეგ კოლოიდური სისტემა აღდგება.
შექცევადი კოაგულაციის მაგალითია კვერცხის ალბუმინის ცილის დალექვა მარილის ხსნარების გავლენით, ხოლო ცილის ნალექი იხსნება ხსნარის განზავებისას ან როდესაც ნალექი გადადის გამოხდილ წყალში.
შეუქცევადი კოაგულაციის მაგალითია ცილის ალბუმინის კოლოიდური სტრუქტურის განადგურება წყლის დუღილამდე გაცხელებისას. სიკვდილის დროს (სრული), ცოცხალი მატერია იქცევა მკვდარ მატერიად მთელი სისტემის შეუქცევადი კოაგულაციის გამო.
ცილების ქიმიური თვისებები ძალიან მრავალფეროვანია ცილის მოლეკულებში დიდი რაოდენობით ფუნქციური ჯგუფების არსებობის გამო, ასევე ცილის მოლეკულებში პეპტიდების და სხვა ბმების არსებობის გამო. ეკოლოგიური და ბიოლოგიური თვალსაზრისით, უდიდესი მნიშვნელობა აქვს ცილის მოლეკულების ჰიდროლიზების უნარს (ეს საბოლოო ჯამში იწვევს ბუნებრივი ალფა ამინომჟავების ნარევს, რომლებიც მონაწილეობდნენ ამ მოლეკულის ფორმირებაში; ამ ნარევში შეიძლება იყოს სხვა ნივთიერებები, თუ ცილა იყო ცილა), დაჟანგვამდე (მისი პროდუქტები შეიძლება იყოს ნახშირორჟანგი, წყალი, აზოტის ნაერთები, მაგალითად, შარდოვანა, ფოსფორის ნაერთები და ა.შ.).
ცილები იწვის „დამწვარი რქის“ ან „დამწვარი ბუმბულის“ სუნის გათავისუფლებით, რაც აუცილებელია გარემოსდაცვითი ექსპერიმენტების ჩატარებისას. ცნობილია ცილაზე სხვადასხვა ფერის რეაქცია (ბიურეტი, ქსანტოპროტეინი და ა.შ.), მათ შესახებ მეტი დეტალები შეგიძლიათ იხილოთ ქიმიის კურსში.
ცილების ეკოლოგიური და ბიოლოგიური ფუნქციების მოკლე აღწერა
აუცილებელია განვასხვავოთ ცილების ეკოლოგიური და ბიოლოგიური როლი უჯრედებში და მთლიანად ორგანიზმში.
ცილების ეკოლოგიური და ბიოლოგიური როლი უჯრედებში
იმის გამო, რომ ცილები (ნუკლეინის მჟავებთან ერთად) სიცოცხლის ნივთიერებებია, მათი ფუნქციები უჯრედებში ძალიან მრავალფეროვანია.
1. ცილის მოლეკულების ყველაზე მნიშვნელოვანი ფუნქციაა სტრუქტურული ფუნქცია, რომელიც მდგომარეობს იმაში, რომ ცილა არის უჯრედის შემქმნელი ყველა სტრუქტურის ყველაზე მნიშვნელოვანი კომპონენტი, რომელშიც ის შედის სხვადასხვა ქიმიური ნაერთების კომპლექსის შემადგენლობაში.
2. ცილა არის ყველაზე მნიშვნელოვანი რეაგენტი ბიოქიმიური რეაქციების უზარმაზარი მრავალფეროვნების დროს, რომელიც უზრუნველყოფს ცოცხალი ნივთიერების ნორმალურ ფუნქციონირებას, ამიტომ მას ახასიათებს რეაგენტის ფუნქცია.
3. ცოცხალ მატერიაში რეაქციები შესაძლებელია მხოლოდ ბიოლოგიური კატალიზატორების - ფერმენტების არსებობისას და როგორც ბიოქიმიური კვლევების შედეგად დადგინდა ისინი ცილოვანი ხასიათისაა, შესაბამისად ცილებიც ასრულებენ კატალიზურ ფუნქციას.
4. საჭიროების შემთხვევაში ორგანიზმებში იჟანგება ცილები და ამავე დროს გამოიყოფა, რის გამოც სინთეზირდება ატფ, ე.ი. ცილები ასევე ასრულებენ ენერგეტიკულ ფუნქციას, მაგრამ იმის გამო, რომ ამ ნივთიერებებს განსაკუთრებული მნიშვნელობა აქვთ ორგანიზმებისთვის (მათი რთული შემადგენლობის გამო), ცილების ენერგეტიკულ ფუნქციას ორგანიზმები ახორციელებენ მხოლოდ კრიტიკულ პირობებში.
5. ცილებს შეუძლიათ შეასრულონ შენახვის ფუნქციაც, რადგან ისინი ორგანიზმების (განსაკუთრებით მცენარეებისთვის) ნივთიერებებისა და ენერგიის ერთგვარი „კონსერვირებული საკვებია“, რაც უზრუნველყოფს მათ საწყის განვითარებას (ცხოველებისთვის - საშვილოსნოსშიდა, მცენარეებისთვის - ემბრიონის განვითარებამდე ახალგაზრდა ორგანიზმის გამოჩენა - ნერგი).
ცილის მთელი რიგი ფუნქციები დამახასიათებელია როგორც უჯრედებისთვის, ასევე მთლიანად ორგანიზმისთვის, ამიტომ ისინი განიხილება ქვემოთ.
ცილების ეკოლოგიური და ბიოლოგიური როლი ორგანიზმებში (ზოგადად)
1. ცილები ქმნიან სპეციალურ სტრუქტურებს უჯრედებსა და ორგანიზმებში (სხვა ნივთიერებებთან ერთად), რომლებსაც შეუძლიათ გარემოდან სიგნალების აღქმა გაღიზიანების სახით, რის გამოც წარმოიქმნება „აგზნების“ მდგომარეობა, რაზეც ორგანიზმი რეაგირებს გარკვეული რეაქცია, ე.ი. ცილებს, როგორც უჯრედში, ისე მთლიანად ორგანიზმში ახასიათებთ აღქმის ფუნქცია.
2. ცილებს ასევე ახასიათებს გამტარი ფუნქცია (როგორც უჯრედებში, ისე მთლიანად ორგანიზმში), რომელიც მდგომარეობს იმაში, რომ უჯრედის (ორგანიზმის) გარკვეულ სტრუქტურებში წარმოქმნილი აგზნება გადაეცემა შესაბამის ცენტრს (უჯრედს). ან ორგანიზმი), რომელშიც წარმოიქმნება ორგანიზმის ან უჯრედის გარკვეული რეაქცია (რეაქცია) მიღებულ სიგნალზე.
3. ბევრ ორგანიზმს შეუძლია სივრცეში გადაადგილება, რაც შესაძლებელია უჯრედის ან ორგანიზმის სტრუქტურების შეკუმშვის უნარის გამო და ეს შესაძლებელია იმიტომ, რომ ფიბრილარული სტრუქტურის ცილებს კუმშვადი ფუნქცია აქვთ.
4. ჰეტეროტროფული ორგანიზმებისთვის ცილები, როგორც ცალ-ცალკე, ისე სხვა ნივთიერებებთან შერევით, წარმოადგენს საკვებ პროდუქტს, ანუ მათ ახასიათებთ ტროფიკული ფუნქცია.
ჰეტეროტროფულ ორგანიზმებში ცილების ტრანსფორმაციების მოკლე აღწერა ადამიანის მაგალითის გამოყენებით
საკვებში შემავალი ცილები შედიან პირის ღრუში, სადაც ატენიანებენ ნერწყვით, კბილებს აჭიანურებენ და გარდაიქმნებიან ერთგვაროვან მასად (სრული ღეჭვით), ხოლო ფარინქსისა და საყლაპავი მილის მეშვეობით კუჭში (სანამ ამ უკანასკნელში არ შევლენ, არაფერი ხდება. ცილები, როგორც ნაერთები).
კუჭში საკვების ბოლუსი გაჯერებულია კუჭის წვენით, რომელიც წარმოადგენს კუჭის ჯირკვლების სეკრეციას. კუჭის წვენი წყალბადის ქლორიდისა და ფერმენტების შემცველი წყალხსნარია, რომელთაგან ყველაზე მნიშვნელოვანია (ცილებისთვის) პეპსინი. პეპსინი მჟავე გარემოში იწვევს ცილების ჰიდროლიზს პეპტონებამდე. შემდეგ საკვები გროვა შედის წვრილი ნაწლავის პირველ ნაწილში - თორმეტგოჯა ნაწლავში, რომელშიც იხსნება პანკრეასის სადინარი, გამოიყოფა პანკრეასის წვენი, რომელსაც აქვს ტუტე გარემო და ფერმენტების კომპლექსი, რომელთაგან ტრიპსინი აჩქარებს ცილის ჰიდროლიზის პროცესს და იწვევს მას. ბოლომდე, ანუ ბუნებრივი ალფა ამინომჟავების ნარევების გაჩენამდე (ისინი ხსნადია და სისხლში შეიწოვება ნაწლავის ჯირკვლებით).
ამინომჟავების ეს ნარევი შედის ინტერსტიციულ სითხეში და იქიდან სხეულის უჯრედებში, რომლებშიც ისინი (ამინომჟავები) შედიან სხვადასხვა ტრანსფორმაციაში. ამ ნაერთების ერთი ნაწილი უშუალოდ გამოიყენება მოცემული ორგანიზმისთვის დამახასიათებელი ცილების სინთეზისთვის, მეორე ექვემდებარება ტრანსამინაციას ან დეამინაციას, აძლევს ორგანიზმისთვის საჭირო ახალ ნაერთებს, მესამე იჟანგება და წარმოადგენს ორგანიზმისთვის საჭირო ენერგიის წყაროს. გააცნობიეროს მისი სასიცოცხლო ფუნქციები.
აუცილებელია აღინიშნოს უჯრედშიდა ცილის ტრანსფორმაციის ზოგიერთი თავისებურება. თუ ორგანიზმი ჰეტეროტროფული და ერთუჯრედულია, მაშინ საკვების ცილები უჯრედებში შედიან ციტოპლაზმაში ან სპეციალურ საჭმლის მომნელებელ ვაკუოლებში, სადაც ისინი განიცდიან ჰიდროლიზს ფერმენტების მოქმედებით, შემდეგ კი ყველაფერი მიდის ისე, როგორც აღწერილია უჯრედებში ამინომჟავებისთვის. უჯრედული სტრუქტურები მუდმივად განახლდება, ამიტომ "ძველი" ცილა იცვლება "ახლით", ხოლო პირველი ჰიდროლიზდება ამინომჟავების ნარევის წარმოქმნით.
ავტოტროფულ ორგანიზმებს აქვთ საკუთარი მახასიათებლები ცილების ტრანსფორმაციაში. პირველადი ცილები (მერისტემულ უჯრედებში) სინთეზირდება ამინომჟავებისგან, რომლებიც სინთეზირდება პირველადი ნახშირწყლების (ისინი ფოტოსინთეზის დროს წარმოქმნილი) და არაორგანული აზოტის შემცველი ნივთიერებების (ნიტრატები ან ამონიუმის მარილები) ტრანსფორმაციის პროდუქტებისგან. აუტოტროფული ორგანიზმების ხანგრძლივ უჯრედებში ცილის სტრუქტურების ჩანაცვლება არ განსხვავდება ჰეტეროტროფული ორგანიზმებისგან.
აზოტის ბალანსი
ცილები, რომლებიც შედგება ამინომჟავებისგან, არის ძირითადი ნაერთები, რომლებიც აუცილებელია სიცოცხლის პროცესებისთვის. აქედან გამომდინარე, ძალზე მნიშვნელოვანია ცილების მეტაბოლიზმისა და მათი დაშლის პროდუქტების გათვალისწინება.
ოფლში ძალიან ცოტა აზოტია, ამიტომ ოფლის ანალიზი აზოტის შემცველობაზე ჩვეულებრივ არ კეთდება. საკვებიდან მიღებული აზოტის რაოდენობა და შარდსა და განავალში შემავალი აზოტის რაოდენობა მრავლდება 6,25-ით (16%) და მეორეს აკლდება პირველი მნიშვნელობა. შედეგად განისაზღვრება ორგანიზმში შეყვანილი და შეწოვილი აზოტის რაოდენობა.
როდესაც საკვებით ორგანიზმში შემავალი აზოტის რაოდენობა უდრის შარდში და განავალში არსებული აზოტის რაოდენობას, ანუ წარმოიქმნება დეამინაციის დროს, მაშინ დგება აზოტის წონასწორობა. აზოტის ბალანსი დამახასიათებელია, როგორც წესი, ჯანმრთელი ზრდასრული ორგანიზმისთვის.
როდესაც ორგანიზმში შემავალი აზოტის რაოდენობა აღემატება გამოყოფილ აზოტის რაოდენობას, მაშინ არის დადებითი აზოტის ბალანსი, ანუ ორგანიზმში შემავალი ცილის რაოდენობა მეტია, ვიდრე დაშლილი ცილის რაოდენობა. მზარდი ჯანსაღი ორგანიზმისთვის დამახასიათებელია აზოტის დადებითი ბალანსი.
როდესაც დიეტური ცილების მიღება იზრდება, იზრდება შარდში გამოყოფილი აზოტის რაოდენობაც.
და ბოლოს, როდესაც ორგანიზმში შემავალი აზოტის რაოდენობა ნაკლებია გამოყოფილ აზოტის რაოდენობაზე, მაშინ ჩნდება უარყოფითი აზოტის ბალანსი, რომლის დროსაც ცილის დაშლა აჭარბებს მის სინთეზს და ორგანიზმის შემადგენელი ცილა ნადგურდება. ეს ხდება ცილოვანი შიმშილის დროს და როცა ორგანიზმისთვის საჭირო ამინომჟავები არ მიეწოდება. უარყოფითი აზოტის ბალანსი ასევე გამოვლინდა მაიონებელი გამოსხივების დიდი დოზების ზემოქმედების შემდეგ, რაც იწვევს ორგანოებსა და ქსოვილებში ცილების დაშლას.
პროტეინის ოპტიმალური პრობლემა
საკვების ცილების მინიმალური რაოდენობა, რომელიც საჭიროა სხეულის გაუარესებული ცილების შესავსებად, ან სხეულის ცილების დაშლის ოდენობა ექსკლუზიურად ნახშირწყლების დიეტით, მითითებულია აცვიათ კოეფიციენტად. ზრდასრულ ადამიანში ამ კოეფიციენტის ყველაზე მცირე მნიშვნელობა შეადგენს დაახლოებით 30 გ ცილას დღეში. თუმცა, ეს რაოდენობა საკმარისი არ არის.
ცხიმები და ნახშირწყლები გავლენას ახდენენ ცილების მოხმარებაზე პლასტიკური მიზნებისთვის საჭირო მინიმუმზე, რადგან ისინი ათავისუფლებენ იმ ენერგიას, რომელიც საჭირო იყო ცილების დაშლისთვის მინიმუმზე მეტი. ნორმალური კვების დროს ნახშირწყლები 3-3,5-ჯერ უფრო მეტად ამცირებს ცილების დაშლას, ვიდრე სრული მარხვის დროს.
საკმარისად ნახშირწყლებისა და ცხიმების შემცველი შერეული საკვებით და 70 კგ სხეულის მასით, ცილის ნორმა დღეში 105გრ.
ცილის რაოდენობა, რომელიც სრულად უზრუნველყოფს ორგანიზმის ზრდას და სასიცოცხლო აქტივობას, განსაზღვრავს ოპტიმალურ პროტეინს და უდრის 100-125 გ პროტეინს დღეში ადამიანისთვის მსუბუქი მუშაობის დროს, 165 გ-მდე დღეში მძიმე სამუშაოს დროს. ხოლო ძალიან მძიმე სამუშაოს დროს 220-230 გ.
ცილის რაოდენობა დღეში უნდა იყოს მთლიანი საკვების მინიმუმ 17% წონის მიხედვით და 14% ენერგიის მიხედვით.
სრული და არასრული ცილები
ცილები, რომლებიც ორგანიზმში შედის საკვებთან ერთად, იყოფა ბიოლოგიურად სრულ და ბიოლოგიურად არასრულად.
ბიოლოგიურად სრული ცილები არის ცილები, რომლებიც შეიცავს საკმარისი რაოდენობით ყველა ამინომჟავას, რომელიც აუცილებელია ცხოველის ორგანიზმში ცილის სინთეზისთვის. სხეულის ზრდისთვის აუცილებელი სრული ცილები მოიცავს შემდეგ აუცილებელ ამინომჟავებს: ლიზინი, ტრიპტოფანი, ტრეონინი, ლეიცინი, იზოლეიცინი, ჰისტიდინი, არგინინი, ვალინი, მეთიონინი, ფენილალანინი. ამ ამინომჟავებიდან შეიძლება წარმოიქმნას სხვა ამინომჟავები, ჰორმონები და ა.შ. ტიროზინი წარმოიქმნება ფენილალანინისგან, ჰორმონები თიროქსინი და ადრენალინი წარმოიქმნება ტრანსფორმაციების გზით, ხოლო ჰისტამინი წარმოიქმნება ჰისტიდინისგან. მეთიონინი მონაწილეობს ფარისებრი ჯირკვლის ჰორმონების ფორმირებაში და აუცილებელია ქოლინის, ცისტეინის და გლუტათიონის ფორმირებისთვის. აუცილებელია რედოქს პროცესებისთვის, აზოტის მეტაბოლიზმისთვის, ცხიმების შეწოვისთვის და ტვინის ნორმალური აქტივობისთვის. ლიზინი მონაწილეობს ჰემატოპოეზში და ხელს უწყობს სხეულის ზრდას. ტრიპტოფანი ასევე აუცილებელია ზრდისთვის, მონაწილეობს სეროტონინის, PP ვიტამინის ფორმირებაში და ქსოვილების სინთეზში. ლიზინი, ცისტინი და ვალინი ასტიმულირებს გულის აქტივობას. საკვებში ცისტინის დაბალი შემცველობა აფერხებს თმის ზრდას და ზრდის სისხლში შაქარს.
ბიოლოგიურად დეფიციტური ცილები არის ცილები, რომლებსაც აკლიათ თუნდაც ერთი ამინომჟავა, რომლის სინთეზირებაც შეუძლებელია ცხოველური ორგანიზმების მიერ.
ცილის ბიოლოგიური ღირებულება იზომება სხეულის ცილის ოდენობით, რომელიც წარმოიქმნება 100 გრ საკვების ცილისგან.
ცხოველური წარმოშობის ცილები, რომლებიც გვხვდება ხორცში, კვერცხსა და რძეში, ყველაზე სრულყოფილია (70-95%). მცენარეული წარმოშობის ცილებს უფრო დაბალი ბიოლოგიური ღირებულება აქვთ, მაგალითად, ჭვავის პურის, სიმინდის (60%), კარტოფილის, საფუარის (67%) ცილებს.
ცხოველური ცილა - ჟელატინი, რომელიც არ შეიცავს ტრიპტოფანს და ტიროზინს, ჩამორჩება. ხორბალი და ქერი დაბალია ლიზინის შემცველობით, ხოლო სიმინდი - ლიზინსა და ტრიპტოფანში.
ზოგიერთი ამინომჟავა ცვლის ერთმანეთს, მაგალითად ფენილალანინი ცვლის ტიროზინს.
ორი არასრული ცილა, რომლებსაც აკლიათ სხვადასხვა ამინომჟავები, ერთად ქმნიან სრულ ცილოვან დიეტას.
ღვიძლის როლი ცილების სინთეზში
ღვიძლი სინთეზირებს სისხლის პლაზმაში შემავალ ცილებს: ალბუმინებს, გლობულინებს (გარდა გამა გლობულინების), ფიბრინოგენს, ნუკლეინის მჟავებს და მრავალფეროვან ფერმენტს, რომელთაგან ზოგიერთი სინთეზირდება მხოლოდ ღვიძლში, მაგალითად ფერმენტები, რომლებიც მონაწილეობენ შარდოვანას წარმოქმნაში.
სხეულში სინთეზირებული ცილები არის ორგანოების, ქსოვილებისა და უჯრედების ნაწილი, ფერმენტები და ჰორმონები (ცილების პლასტიკური მნიშვნელობა), მაგრამ არ ინახება ორგანიზმის მიერ სხვადასხვა ცილის ნაერთების სახით. ამრიგად, ცილების ის ნაწილი, რომელსაც არ აქვს პლასტიკური მნიშვნელობა, დეამინირებულია ფერმენტების მონაწილეობით - იშლება ენერგიის გამოყოფით სხვადასხვა აზოტოვან პროდუქტებში. ღვიძლის ცილების ნახევარგამოყოფის პერიოდი შეადგენს 10 დღეს.
ცილოვანი კვება სხვადასხვა პირობებში
მოუნელებელი ცილა არ შეიწოვება ორგანიზმის მიერ, გარდა საჭმლის მომნელებელი არხისა. საჭმლის მომნელებელი არხის გარეთ შეყვანილი ცილა (პარენტერალურად) იწვევს ორგანიზმის დამცავ რეაქციას.
დაშლილი ცილის ამინომჟავები და მათი ნაერთები - პოლიპეპტიდები - შედიან სხეულის უჯრედებში, რომლებშიც ფერმენტების გავლენით ცილის სინთეზი განუწყვეტლივ ხდება მთელი ცხოვრების მანძილზე. საკვების ცილებს ძირითადად პლასტიკური მნიშვნელობა აქვთ.
ორგანიზმის ზრდის პერიოდში - ბავშვობაში და მოზარდობაში - ცილების სინთეზი განსაკუთრებით მაღალია. სიბერეში ცილების სინთეზი მცირდება. შესაბამისად, ზრდის პროცესის დროს ხდება ცილების შემადგენელი ქიმიკატების ორგანიზმში შეკავება.
იზოტოპების გამოყენებით მეტაბოლიზმის შესწავლამ აჩვენა, რომ ზოგიერთ ორგანოში, 2-3 დღის განმავლობაში, ცილების დაახლოებით ნახევარი განიცდის დაშლას და იგივე რაოდენობის ცილები ახლად სინთეზირდება ორგანიზმის მიერ (რესინთეზი). თითოეულში, თითოეულ ორგანიზმში სინთეზირდება სპეციფიკური ცილები, რომლებიც განსხვავდება სხვა ქსოვილებისა და სხვა ორგანიზმების ცილებისგან.
ცხიმებისა და ნახშირწყლების მსგავსად, ამინომჟავები, რომლებიც არ გამოიყენება სხეულის ასაშენებლად, იშლება ენერგიის გასათავისუფლებლად.
ამინომჟავები, რომლებიც წარმოიქმნება სხეულის მომაკვდავი, კოლაფსირებული უჯრედების ცილებისგან, ასევე განიცდის ტრანსფორმაციას ენერგიის განთავისუფლებით.
ნორმალურ პირობებში ზრდასრული ადამიანისთვის დღეში მოთხოვნილი ცილის რაოდენობა შეადგენს 1,5-2,0 გ 1 კგ წონაზე, ხანგრძლივი სიცივის პირობებში 3,0-3,5 გ, ძალიან მძიმე ფიზიკური შრომით 3,0-3,5 გ.
ცილების რაოდენობის მატება 3,0-3,5 გ-ზე მეტი 1 კგ წონაზე არღვევს ნერვული სისტემის, ღვიძლისა და თირკმელების აქტივობას.
ლიპიდები, მათი კლასიფიკაცია და ფიზიოლოგიური როლი
ლიპიდები არის ნივთიერებები, რომლებიც არ იხსნება წყალში და იხსნება ორგანულ ნაერთებში (ალკოჰოლი, ქლოროფორმი და ა.შ.). ლიპიდებში შედის ნეიტრალური ცხიმები, ცხიმის მსგავსი ნივთიერებები (ლიპოიდები) და ზოგიერთი ვიტამინი (A, D, E, K). ლიპიდებს აქვთ პლასტიკური მნიშვნელობა და ყველა უჯრედისა და სასქესო ჰორმონის ნაწილია.
განსაკუთრებით ბევრი ლიპიდებია ნერვული სისტემის და თირკმელზედა ჯირკვლების უჯრედებში. მათ მნიშვნელოვან ნაწილს ორგანიზმი იყენებს ენერგეტიკულ მასალად.
ამინომჟავები ბუნებრივი პოლიპეპტიდები და ცილები მოიცავს ამინომჟავებს, რომელთა მოლეკულებში ამინო და კარბოქსილის ჯგუფები დაკავშირებულია იმავე ნახშირბადის ატომთან. H 2 N–CH–COOH R ნახშირწყალბადის რადიკალი R სტრუქტურიდან გამომდინარე, ბუნებრივი ამინომჟავები იყოფა ალიფატურ, არომატულ და ჰეტეროციკლურებად. ალიფატური ამინომჟავები შეიძლება იყოს არაპოლარული (ჰიდროფობიური), პოლარული დაუხტვილი ან პოლარული დამუხტული. რადიკალში ფუნქციური ჯგუფების შემცველობიდან გამომდინარე, განასხვავებენ ჰიდროქსილის, ამიდის, კარბოქსილის და ამინო ჯგუფების შემცველ ამინომჟავებს. როგორც წესი, გამოიყენება ამინომჟავების ტრივიალური სახელები, რომლებიც ჩვეულებრივ ასოცირდება მათი იზოლაციის წყაროებთან ან თვისებებთან.
 -ამინომჟავების კლასიფიკაცია ნახშირწყალბადის რადიკალის სტრუქტურის მიხედვით ალიფატური არაპოლარული რადიკალი H –CH–COOH NH 2 CH 3 –CH–COOH გლიცინი NH 2 CH 3 CH –CH–COOH CH 3 NH 2 ალანინი CH 3 CH CH 2– CH–COOH ვალინი CH 3 CH 2 CH–CH–COOH H 3 C NH 2 იზოლეიცინი NH 2 ლეიცინი ალიფატური პოლარული რადიკალი CH 2 –CH–COOH OH NH 2 HS–CH 2 –CH–COOH CH 3 CH –CH–COOH სერინი OH NH 2 CH 2 – CH–COOH NH 2 ცისტეინი ტრეონინი SCH 3 NH 2 მეთიონინი CH 2 CH 2 –CH–COOH CH 2 –– CH–COOH СONН 2 NH 2 გლუტამინი COOH NH 2 ასპარტინის მჟავა NH 2 გლუტა 2 –CH–COOH NH 2 NH 2 ლიზინი CH 2 –– CH–COOH H 2 N–C–NH–CH 2 –CH–COOH NH СONН 2 NH 2 ასპარაგინი NH 2 არგინინი არომატული და ჰეტეროციკლური რადიკალები ––CH –CH– COOH ჰეტეროციკლური რადიკალი –CH–COOH HO – –CH–COOH HN N NH COOH კარბოციკლური რადიკალი ტიროზინი NH ფენილალანინი NH 2 2 2 ჰისტიდინი N–H პროლინი
-ამინომჟავების კლასიფიკაცია ნახშირწყალბადის რადიკალის სტრუქტურის მიხედვით ალიფატური არაპოლარული რადიკალი H –CH–COOH NH 2 CH 3 –CH–COOH გლიცინი NH 2 CH 3 CH –CH–COOH CH 3 NH 2 ალანინი CH 3 CH CH 2– CH–COOH ვალინი CH 3 CH 2 CH–CH–COOH H 3 C NH 2 იზოლეიცინი NH 2 ლეიცინი ალიფატური პოლარული რადიკალი CH 2 –CH–COOH OH NH 2 HS–CH 2 –CH–COOH CH 3 CH –CH–COOH სერინი OH NH 2 CH 2 – CH–COOH NH 2 ცისტეინი ტრეონინი SCH 3 NH 2 მეთიონინი CH 2 CH 2 –CH–COOH CH 2 –– CH–COOH СONН 2 NH 2 გლუტამინი COOH NH 2 ასპარტინის მჟავა NH 2 გლუტა 2 –CH–COOH NH 2 NH 2 ლიზინი CH 2 –– CH–COOH H 2 N–C–NH–CH 2 –CH–COOH NH СONН 2 NH 2 ასპარაგინი NH 2 არგინინი არომატული და ჰეტეროციკლური რადიკალები ––CH –CH– COOH ჰეტეროციკლური რადიკალი –CH–COOH HO – –CH–COOH HN N NH COOH კარბოციკლური რადიკალი ტიროზინი NH ფენილალანინი NH 2 2 2 ჰისტიდინი N–H პროლინი
 შესაცვლელი და შეუცვლელი ამინომჟავები ყველა ბუნებრივი ამინომჟავა იყოფა არსებით, რომელიც ორგანიზმში შემოდის მხოლოდ გარე გარემოდან და არაარსებით, რომელთა სინთეზი ხდება ორგანიზმში. აუცილებელი ამინომჟავები: არსებითი ამინომჟავები: ვალინი, ლეიცინი, იზოლეიცინი, გლიცინი, ალანინი, პროლინი, ლიზინი, მეთიონინი, ტრეონინი, სერინი, ცისტეინი, არგინინი, ჰისტიდინი, ტრიპტოფანი, ფენილალანინი ასპარაგინი, გლუტამინი, ასპარატინის მჟავა და საწყისი მასალები. ამინომჟავების ბიოსინთეზი შეიძლება იმოქმედოს სხვა ამინომჟავებმა, ისევე როგორც ნივთიერებები, რომლებიც მიეკუთვნებიან ორგანული ნაერთების სხვა კლასებს (მაგალითად, კეტომჟავები არიან ამ პროცესის კატალიზატორები და მონაწილეები). სხვადასხვა ცილების ამინომჟავების შემადგენლობის ანალიზი აჩვენებს, რომ დიკარბოქსილის მჟავების და მათი ამიდების წილი ცილების უმეტესობაში შეადგენს ყველა ამინომჟავების 25-27%-ს. ეს იგივე ამინომჟავები, ლეიცინთან და ლიზინთან ერთად, შეადგენს ყველა ცილის ამინომჟავების დაახლოებით 50%-ს. ამავდროულად, ამინომჟავების წილი, როგორიცაა ცისტეინი, მეთიონინი, ტრიპტოფანი, ჰისტიდინი შეადგენს არაუმეტეს 1,5 - 3,5%.
შესაცვლელი და შეუცვლელი ამინომჟავები ყველა ბუნებრივი ამინომჟავა იყოფა არსებით, რომელიც ორგანიზმში შემოდის მხოლოდ გარე გარემოდან და არაარსებით, რომელთა სინთეზი ხდება ორგანიზმში. აუცილებელი ამინომჟავები: არსებითი ამინომჟავები: ვალინი, ლეიცინი, იზოლეიცინი, გლიცინი, ალანინი, პროლინი, ლიზინი, მეთიონინი, ტრეონინი, სერინი, ცისტეინი, არგინინი, ჰისტიდინი, ტრიპტოფანი, ფენილალანინი ასპარაგინი, გლუტამინი, ასპარატინის მჟავა და საწყისი მასალები. ამინომჟავების ბიოსინთეზი შეიძლება იმოქმედოს სხვა ამინომჟავებმა, ისევე როგორც ნივთიერებები, რომლებიც მიეკუთვნებიან ორგანული ნაერთების სხვა კლასებს (მაგალითად, კეტომჟავები არიან ამ პროცესის კატალიზატორები და მონაწილეები). სხვადასხვა ცილების ამინომჟავების შემადგენლობის ანალიზი აჩვენებს, რომ დიკარბოქსილის მჟავების და მათი ამიდების წილი ცილების უმეტესობაში შეადგენს ყველა ამინომჟავების 25-27%-ს. ეს იგივე ამინომჟავები, ლეიცინთან და ლიზინთან ერთად, შეადგენს ყველა ცილის ამინომჟავების დაახლოებით 50%-ს. ამავდროულად, ამინომჟავების წილი, როგორიცაა ცისტეინი, მეთიონინი, ტრიპტოფანი, ჰისტიდინი შეადგენს არაუმეტეს 1,5 - 3,5%.
 -ამინომჟავების სტერეოიზომერიზმი სივრცითი ან სტერეოიზომერები ან ოპტიკურად აქტიური ნაერთები არის ნაერთები, რომლებიც შეიძლება არსებობდეს სივრცეში ორი იზომერის სახით, რომლებიც ერთმანეთის სარკისებური გამოსახულებაა (ენანტიომერები). ყველა α-ამინომჟავა, გარდა გლიცინისა, არის ოპტიკურად აქტიური ნაერთები და შეუძლია ბრუნოს სიბრტყით პოლარიზებული სინათლის პოლარიზაციის სიბრტყე (რომლის ყველა ტალღა ვიბრირებს იმავე სიბრტყეში) მარჯვნივ (+, დექსტროროტორული) ან მარცხნივ (- , მარცხნივ). ოპტიკური აქტივობის ნიშნები: - ნახშირბადის ასიმეტრიული ატომის მოლეკულაში არსებობა (ატომი, რომელიც დაკავშირებულია ოთხ სხვადასხვა შემცვლელთან); - სიმეტრიის ელემენტების არარსებობა მოლეკულაში. α-ამინომჟავების ენანტიომერები ჩვეულებრივ გამოსახულია ფარდობითი კონფიგურაციების სახით და დასახელებულია D, L ნომენკლატურით.
-ამინომჟავების სტერეოიზომერიზმი სივრცითი ან სტერეოიზომერები ან ოპტიკურად აქტიური ნაერთები არის ნაერთები, რომლებიც შეიძლება არსებობდეს სივრცეში ორი იზომერის სახით, რომლებიც ერთმანეთის სარკისებური გამოსახულებაა (ენანტიომერები). ყველა α-ამინომჟავა, გარდა გლიცინისა, არის ოპტიკურად აქტიური ნაერთები და შეუძლია ბრუნოს სიბრტყით პოლარიზებული სინათლის პოლარიზაციის სიბრტყე (რომლის ყველა ტალღა ვიბრირებს იმავე სიბრტყეში) მარჯვნივ (+, დექსტროროტორული) ან მარცხნივ (- , მარცხნივ). ოპტიკური აქტივობის ნიშნები: - ნახშირბადის ასიმეტრიული ატომის მოლეკულაში არსებობა (ატომი, რომელიც დაკავშირებულია ოთხ სხვადასხვა შემცვლელთან); - სიმეტრიის ელემენტების არარსებობა მოლეკულაში. α-ამინომჟავების ენანტიომერები ჩვეულებრივ გამოსახულია ფარდობითი კონფიგურაციების სახით და დასახელებულია D, L ნომენკლატურით.
 -ამინომჟავების შედარებითი კონფიგურაციები ალანინის მოლეკულაში ნახშირბადის მეორე ატომი ასიმეტრიულია (მას აქვს 4 განსხვავებული შემცვლელი: წყალბადის ატომი, კარბოქსილი, მეთილი და ამინო ჯგუფები. მოლეკულის ნახშირწყალბადის ჯაჭვი მოთავსებულია ვერტიკალურად, მხოლოდ ატომები და ჯგუფებია დაკავშირებული. ასიმეტრიული ნახშირბადის ატომით გამოსახულია სარკისებური გამოსახულება, რადგან ამინომჟავები, როგორც წესი, არის წყალბადის ატომი და ამინო ჯგუფი, რომელიც მდებარეობს ნახშირბადის ჯაჭვის მარჯვნივ. ეს არის COOH H–C– NH 2 CH 3 D–ალანინი COOH H 2 N–H CH 3 L–ალანინი ბუნებრივი ცილები შეიცავს ამინომჟავების მხოლოდ L იზომერებს სიბრტყით პოლარიზებული სინათლის პოლარიზაციის სიბრტყეზე ოდნავ მეტი L ამინომჟავა არის დექსტროროტაციული (ალანინი, იზოლეიცინი, გლუტამინის მჟავა, ლიზინი და ა.შ.);
-ამინომჟავების შედარებითი კონფიგურაციები ალანინის მოლეკულაში ნახშირბადის მეორე ატომი ასიმეტრიულია (მას აქვს 4 განსხვავებული შემცვლელი: წყალბადის ატომი, კარბოქსილი, მეთილი და ამინო ჯგუფები. მოლეკულის ნახშირწყალბადის ჯაჭვი მოთავსებულია ვერტიკალურად, მხოლოდ ატომები და ჯგუფებია დაკავშირებული. ასიმეტრიული ნახშირბადის ატომით გამოსახულია სარკისებური გამოსახულება, რადგან ამინომჟავები, როგორც წესი, არის წყალბადის ატომი და ამინო ჯგუფი, რომელიც მდებარეობს ნახშირბადის ჯაჭვის მარჯვნივ. ეს არის COOH H–C– NH 2 CH 3 D–ალანინი COOH H 2 N–H CH 3 L–ალანინი ბუნებრივი ცილები შეიცავს ამინომჟავების მხოლოდ L იზომერებს სიბრტყით პოლარიზებული სინათლის პოლარიზაციის სიბრტყეზე ოდნავ მეტი L ამინომჟავა არის დექსტროროტაციული (ალანინი, იზოლეიცინი, გლუტამინის მჟავა, ლიზინი და ა.შ.);
 ამინომჟავების კონფიგურაცია განსაზღვრავს როგორც თავად ამინომჟავების, ისე ბიოპოლიმერების სივრცულ სტრუქტურას და ბიოლოგიურ თვისებებს - ცილები, რომლებიც აგებულია ამინომჟავების ნარჩენებისგან. ზოგიერთი ამინომჟავისთვის არსებობს კავშირი მათ კონფიგურაციასა და გემოს შორის, მაგალითად, L Trp, L Phen, L Tyr, L Leu აქვთ მწარე გემო, ხოლო მათი D ენანტიომერები ტკბილია. გლიცინის ტკბილი გემო დიდი ხანია ცნობილია. ტრეონინის L იზომერი ზოგისთვის ტკბილია, ზოგისთვის კი მწარე. გლუტამინის მჟავას მონონატრიუმის მარილი, მონოსტრიუმის გლუტამატი არის გემოვნების თვისებების ერთ-ერთი ყველაზე მნიშვნელოვანი მატარებელი, რომელიც გამოიყენება კვების მრეწველობაში. საინტერესოა აღინიშნოს, რომ ასპარტინის მჟავისა და ფენილალანინის დიპეპტიდური წარმოებული ავლენს ინტენსიურად ტკბილ გემოს. ყველა ამინომჟავა არის თეთრი კრისტალური ნივთიერებები ძალიან მაღალი ტემპერატურით (230 ° C-ზე მეტი). მჟავების უმეტესობა წყალში ძალიან ხსნადია და პრაქტიკულად უხსნადია ალკოჰოლში და დიეთილის ეთერში. ეს, ისევე როგორც მაღალი დნობის წერტილი, მიუთითებს ამ ნივთიერებების მარილიან ბუნებაზე. ამინომჟავების სპეციფიკური ხსნადობა განპირობებულია მოლეკულაში როგორც ამინო ჯგუფის (ძირითადი ხასიათი), ასევე კარბოქსილის ჯგუფის (მჟავე თვისებები) არსებობით, რის გამოც ამინომჟავები მიეკუთვნება ამფოტერულ ელექტროლიტებს (ამფოლიტებს).
ამინომჟავების კონფიგურაცია განსაზღვრავს როგორც თავად ამინომჟავების, ისე ბიოპოლიმერების სივრცულ სტრუქტურას და ბიოლოგიურ თვისებებს - ცილები, რომლებიც აგებულია ამინომჟავების ნარჩენებისგან. ზოგიერთი ამინომჟავისთვის არსებობს კავშირი მათ კონფიგურაციასა და გემოს შორის, მაგალითად, L Trp, L Phen, L Tyr, L Leu აქვთ მწარე გემო, ხოლო მათი D ენანტიომერები ტკბილია. გლიცინის ტკბილი გემო დიდი ხანია ცნობილია. ტრეონინის L იზომერი ზოგისთვის ტკბილია, ზოგისთვის კი მწარე. გლუტამინის მჟავას მონონატრიუმის მარილი, მონოსტრიუმის გლუტამატი არის გემოვნების თვისებების ერთ-ერთი ყველაზე მნიშვნელოვანი მატარებელი, რომელიც გამოიყენება კვების მრეწველობაში. საინტერესოა აღინიშნოს, რომ ასპარტინის მჟავისა და ფენილალანინის დიპეპტიდური წარმოებული ავლენს ინტენსიურად ტკბილ გემოს. ყველა ამინომჟავა არის თეთრი კრისტალური ნივთიერებები ძალიან მაღალი ტემპერატურით (230 ° C-ზე მეტი). მჟავების უმეტესობა წყალში ძალიან ხსნადია და პრაქტიკულად უხსნადია ალკოჰოლში და დიეთილის ეთერში. ეს, ისევე როგორც მაღალი დნობის წერტილი, მიუთითებს ამ ნივთიერებების მარილიან ბუნებაზე. ამინომჟავების სპეციფიკური ხსნადობა განპირობებულია მოლეკულაში როგორც ამინო ჯგუფის (ძირითადი ხასიათი), ასევე კარბოქსილის ჯგუფის (მჟავე თვისებები) არსებობით, რის გამოც ამინომჟავები მიეკუთვნება ამფოტერულ ელექტროლიტებს (ამფოლიტებს).
 ამინომჟავების მჟავა-ტუტოვანი თვისებები ამინომჟავები შეიცავს როგორც მჟავე კარბოქსილის ჯგუფს, ასევე ძირითად ამინო ჯგუფს. წყალხსნარებში და მყარ მდგომარეობაში ამინომჟავები არსებობს მხოლოდ შიდა მარილების სახით - ცვიტერული იონები ან ბიპოლარული იონები. ამინომჟავის მჟავა-ტუტოვანი წონასწორობა შეიძლება აღწერილი იყოს: CH 3 –CH–COO - OH– NH 2 H+ ანიონი CH 3 –CH–COO– H+ +NH 3 ბიპოლარული OH- იონი CH 3 –CH–COOH +NH 3 კატიონი B მჟავე გარემოში ამინომჟავის მოლეკულები კატიონია. როდესაც ელექტრული დენი გადის ასეთ ხსნარში, ამინომჟავის კათიონები გადადიან კათოდში და იქ მცირდება. ტუტე გარემოში ამინომჟავის მოლეკულები არის ანიონი. როდესაც ელექტრული დენი გადის ასეთ ხსნარში, ამინომჟავის ანიონები გადადიან ანოდში და იქ იჟანგება. p მნიშვნელობა H, რომელშიც თითქმის ყველა ამინომჟავის მოლეკულა არის ბიპოლარული იონი, ეწოდება იზოელექტრული წერტილი (გვ. I). ამ მნიშვნელობაზე პ. ამინომჟავის ხსნარი არ ატარებს ელექტრო დენს.
ამინომჟავების მჟავა-ტუტოვანი თვისებები ამინომჟავები შეიცავს როგორც მჟავე კარბოქსილის ჯგუფს, ასევე ძირითად ამინო ჯგუფს. წყალხსნარებში და მყარ მდგომარეობაში ამინომჟავები არსებობს მხოლოდ შიდა მარილების სახით - ცვიტერული იონები ან ბიპოლარული იონები. ამინომჟავის მჟავა-ტუტოვანი წონასწორობა შეიძლება აღწერილი იყოს: CH 3 –CH–COO - OH– NH 2 H+ ანიონი CH 3 –CH–COO– H+ +NH 3 ბიპოლარული OH- იონი CH 3 –CH–COOH +NH 3 კატიონი B მჟავე გარემოში ამინომჟავის მოლეკულები კატიონია. როდესაც ელექტრული დენი გადის ასეთ ხსნარში, ამინომჟავის კათიონები გადადიან კათოდში და იქ მცირდება. ტუტე გარემოში ამინომჟავის მოლეკულები არის ანიონი. როდესაც ელექტრული დენი გადის ასეთ ხსნარში, ამინომჟავის ანიონები გადადიან ანოდში და იქ იჟანგება. p მნიშვნელობა H, რომელშიც თითქმის ყველა ამინომჟავის მოლეკულა არის ბიპოლარული იონი, ეწოდება იზოელექტრული წერტილი (გვ. I). ამ მნიშვნელობაზე პ. ამინომჟავის ხსნარი არ ატარებს ელექტრო დენს.
 p მნიშვნელობები. I ყველაზე მნიშვნელოვანი α-ამინომჟავები ცისტეინი (Cys) ასპარაგინი (Asp) ფენილალანინი (Phe) ტრეონინი (Thr) გლუტამინი (Gln) სერინი (Ser) ტიროზინი (Tyr) მეთიონინი (Met) ტრიპტოფანი (Trp) ალანინი (Ala) ვალინი (Val) გლიცინი (Gly) ლეიცინი (Leu) იზოლეიცინი (Ile) პროლინი (Pro) 5, 0 5, 4 5, 5 5, 6 5, 7 5, 8 5, 9 6, 0 6, 1 6, 3 ასპარტიკი მჟავა (Asp) გლუტამინის მჟავა (Glu) ჰისტიდინი (His) ლიზინი (Lys) არგინინი (Arg) 3.0 3.2 7.6 9.8 10.8
p მნიშვნელობები. I ყველაზე მნიშვნელოვანი α-ამინომჟავები ცისტეინი (Cys) ასპარაგინი (Asp) ფენილალანინი (Phe) ტრეონინი (Thr) გლუტამინი (Gln) სერინი (Ser) ტიროზინი (Tyr) მეთიონინი (Met) ტრიპტოფანი (Trp) ალანინი (Ala) ვალინი (Val) გლიცინი (Gly) ლეიცინი (Leu) იზოლეიცინი (Ile) პროლინი (Pro) 5, 0 5, 4 5, 5 5, 6 5, 7 5, 8 5, 9 6, 0 6, 1 6, 3 ასპარტიკი მჟავა (Asp) გლუტამინის მჟავა (Glu) ჰისტიდინი (His) ლიზინი (Lys) არგინინი (Arg) 3.0 3.2 7.6 9.8 10.8
 -ამინომჟავების ქიმიური თვისებები კარბოქსილის ჯგუფთან დაკავშირებული რეაქციები ამინოჯგუფის შემცველი რეაქციები მჟავის ნახშირწყალბადის რადიკალთან დაკავშირებული რეაქციები კარბოქსილის და ამინო ჯგუფის ერთდროული მონაწილეობით
-ამინომჟავების ქიმიური თვისებები კარბოქსილის ჯგუფთან დაკავშირებული რეაქციები ამინოჯგუფის შემცველი რეაქციები მჟავის ნახშირწყალბადის რადიკალთან დაკავშირებული რეაქციები კარბოქსილის და ამინო ჯგუფის ერთდროული მონაწილეობით
 რეაქციები, რომლებიც მოიცავს ამინომჟავების კარბოქსილის ჯგუფს ამინომჟავებს შეუძლიათ შევიდნენ იმავე ქიმიურ რეაქციებში და მისცეს იგივე წარმოებულები, როგორც სხვა კარბოქსილის მჟავები. CH 3 –CH–COOH Na. OH CH 3 –CH–COONa NH 2 CH 3 –CH–COOH NH 2 CH 3 OH NH 3 NH 2 t NH 2 CH 3 –CH–CONH 2 NH 2 ალანინის ამიდი ორგანიზმში ერთ-ერთი ყველაზე მნიშვნელოვანი რეაქციაა დეკარბოქსილაცია. ამინომჟავების. როდესაც CO 2 გამოიყოფა სპეციალური დეკარბოქსილაზას ფერმენტების მოქმედებით, ამინომჟავები გარდაიქმნება ამინებად: CH 2 –CH–COOH NH 2 გლუტამინის მჟავა + H 2 O ალანინის მეთილის ესტერი CH 3 –CH–COO– NH 4+ NH 2 CH 3 –CH–COOCH 3 H+ CH 3 –CH–COOH + H 2 O ალანინის ნატრიუმის მარილი CH 2 –CH 2 NH 2 –CO 2 –ამინობუტირის მჟავა (GABA) მოქმედებს როგორც ნეიროტრანსმიტერი COOH რეაქციები ნახშირწყალბადის რადიკალზე: დაჟანგვა, უფრო სწორად, ფენილალანინის ჰიდროქსილაცია: –CH 2 –CH–COOH NH 2 ფენილალანინი [O] HO– –CH 2 –CH–COOH NH 2 ტიროზინი
რეაქციები, რომლებიც მოიცავს ამინომჟავების კარბოქსილის ჯგუფს ამინომჟავებს შეუძლიათ შევიდნენ იმავე ქიმიურ რეაქციებში და მისცეს იგივე წარმოებულები, როგორც სხვა კარბოქსილის მჟავები. CH 3 –CH–COOH Na. OH CH 3 –CH–COONa NH 2 CH 3 –CH–COOH NH 2 CH 3 OH NH 3 NH 2 t NH 2 CH 3 –CH–CONH 2 NH 2 ალანინის ამიდი ორგანიზმში ერთ-ერთი ყველაზე მნიშვნელოვანი რეაქციაა დეკარბოქსილაცია. ამინომჟავების. როდესაც CO 2 გამოიყოფა სპეციალური დეკარბოქსილაზას ფერმენტების მოქმედებით, ამინომჟავები გარდაიქმნება ამინებად: CH 2 –CH–COOH NH 2 გლუტამინის მჟავა + H 2 O ალანინის მეთილის ესტერი CH 3 –CH–COO– NH 4+ NH 2 CH 3 –CH–COOCH 3 H+ CH 3 –CH–COOH + H 2 O ალანინის ნატრიუმის მარილი CH 2 –CH 2 NH 2 –CO 2 –ამინობუტირის მჟავა (GABA) მოქმედებს როგორც ნეიროტრანსმიტერი COOH რეაქციები ნახშირწყალბადის რადიკალზე: დაჟანგვა, უფრო სწორად, ფენილალანინის ჰიდროქსილაცია: –CH 2 –CH–COOH NH 2 ფენილალანინი [O] HO– –CH 2 –CH–COOH NH 2 ტიროზინი
 რეაქციები, რომლებიც მოიცავს ამინომჟავების ამინო ჯგუფს სხვა ალიფატური ამინების მსგავსად, ამინომჟავებს შეუძლიათ რეაგირება მჟავებთან, ანჰიდრიდებთან და მჟავა ქლორიდებთან და აზოტის მჟავასთან. CH 3 –CH–COOH HCl CH 3 –CH–COOH NH 2 +NH CH 3 –CH–COOH NH 2 CH 3 COCl –HCl CH 33–CH–COOH CH –CH–COOH 3 Cl– ალანინის ქლორიდი CH 3 –CH –COOH NH–CO–CH 3 HNO 22 HNO 2-აცეტილამინოპროპანური მჟავა CH 33–CH–COOH CH –CH–COOH + N 22+ H 22 O + N + HO OH 2 -ჰიდროქსიპროპანური მჟავა NH 22 NH ამინომჟავების გაცხელებისას , რეაქცია ხდება ინტერმოლეკულური დეჰიდრატაცია, რომელიც მოიცავს როგორც ამინო, ასევე კარბოქსილის ჯგუფებს. შედეგი არის ციკლური დიკეტოპიპერაზინის ფორმირება. 2 CH 3 –CH–COOH NH 2 t – 2 H 2 O CH 3 –CH–CO–NH HN––CO–CH–CH 3 დიკეტოპიპერაზინ ალანინი
რეაქციები, რომლებიც მოიცავს ამინომჟავების ამინო ჯგუფს სხვა ალიფატური ამინების მსგავსად, ამინომჟავებს შეუძლიათ რეაგირება მჟავებთან, ანჰიდრიდებთან და მჟავა ქლორიდებთან და აზოტის მჟავასთან. CH 3 –CH–COOH HCl CH 3 –CH–COOH NH 2 +NH CH 3 –CH–COOH NH 2 CH 3 COCl –HCl CH 33–CH–COOH CH –CH–COOH 3 Cl– ალანინის ქლორიდი CH 3 –CH –COOH NH–CO–CH 3 HNO 22 HNO 2-აცეტილამინოპროპანური მჟავა CH 33–CH–COOH CH –CH–COOH + N 22+ H 22 O + N + HO OH 2 -ჰიდროქსიპროპანური მჟავა NH 22 NH ამინომჟავების გაცხელებისას , რეაქცია ხდება ინტერმოლეკულური დეჰიდრატაცია, რომელიც მოიცავს როგორც ამინო, ასევე კარბოქსილის ჯგუფებს. შედეგი არის ციკლური დიკეტოპიპერაზინის ფორმირება. 2 CH 3 –CH–COOH NH 2 t – 2 H 2 O CH 3 –CH–CO–NH HN––CO–CH–CH 3 დიკეტოპიპერაზინ ალანინი
 რეაქციები, რომლებიც მოიცავს ამინო ჯგუფებს - ამინომჟავები დეამინირების რეაქციები. ოქსიდაციური დეამინაცია CH 3 –CH–COOH [O] NH 2 CH 3 –C – COOH + NH 3 პირუვიკ O მჟავის რედუქციური დეამინაცია CH 3 –CH–COOH [H] NH 2 CH 3 –CH 2 – COOH პროპანური მჟავა + NH 3 ჰიდროლიზური დეამინაცია CH 3 –CH–COOH NH 2 H 2 O CH 3 –CH–COOH რძემჟავა HO მჟავა + NH 3 ინტრამოლეკულური დეამინაცია CH 3 –CH–COOH NH 2 CH 2 = CH – COOH პროპენოინის მჟავა + NH 3 ტრანსამინაციის რეაქცია. CH 3 –CH–COOH NH 2 HOOC–CH 2–C – COOH + კეტოგლუტარის მჟავა O CH 3 –C–COOH O HOOC–CH 2–CH– COOH NH 2
რეაქციები, რომლებიც მოიცავს ამინო ჯგუფებს - ამინომჟავები დეამინირების რეაქციები. ოქსიდაციური დეამინაცია CH 3 –CH–COOH [O] NH 2 CH 3 –C – COOH + NH 3 პირუვიკ O მჟავის რედუქციური დეამინაცია CH 3 –CH–COOH [H] NH 2 CH 3 –CH 2 – COOH პროპანური მჟავა + NH 3 ჰიდროლიზური დეამინაცია CH 3 –CH–COOH NH 2 H 2 O CH 3 –CH–COOH რძემჟავა HO მჟავა + NH 3 ინტრამოლეკულური დეამინაცია CH 3 –CH–COOH NH 2 CH 2 = CH – COOH პროპენოინის მჟავა + NH 3 ტრანსამინაციის რეაქცია. CH 3 –CH–COOH NH 2 HOOC–CH 2–C – COOH + კეტოგლუტარის მჟავა O CH 3 –C–COOH O HOOC–CH 2–CH– COOH NH 2
 პეპტიდური კავშირის ფორმირება ამინომჟავების ამინო და კარბოქსილის ჯგუფებს შეუძლიათ ურთიერთქმედება ერთმანეთთან ციკლის წარმოქმნის გარეშე: H 2 N –CH–COOH + H 2 N –CH–COOH CH 3 CH 2 OH H 2 N –CH–CO– NH –CH– COOH –H 2 O CH 3 CH 2 OH დიპეპტიდი ალანინი სერინი ალანილსერინი მიღებულ –CO–NH– კავშირს ეწოდება პეპტიდური ბმა, ხოლო ამინომჟავების ურთიერთქმედების პროდუქტს – პეპტიდი. თუ 2 ამინომჟავა რეაგირებს, მიიღება დიპეპტიდი; 3 ამინომჟავა - ტრიპეპტიდი და ა.შ. პეპტიდებს, რომელთა მოლეკულური წონა არ აღემატება 10000-ს, ეწოდება ოლიგოპეპტიდები, 10000-ზე მეტი მოლეკულური მასით - პოლიპეპტიდები, ანუ ცილები. პეპტიდების შემადგენლობაში არსებული პეპტიდური ბმები ქიმიური ბუნებით ამიდურია. პოლიპეპტიდური ჯაჭვი შედგება რეგულარულად განმეორებადი მონაკვეთებისგან, რომლებიც ქმნიან მოლეკულის ხერხემალს და ცვლადი სექციებისაგან - ამინომჟავების ნარჩენების გვერდითი რადიკალები. პოლიპეპტიდური ჯაჭვის დასაწყისი ითვლება დასასრულად, რომელსაც აქვს თავისუფალი ამინო ჯგუფი (N ბოლო), ხოლო პოლიპეპტიდური ჯაჭვი მთავრდება თავისუფალი კარბოქსილის ჯგუფით (C ბოლო). პეპტიდს ასახელებენ პეპტიდში შემავალი ამინომჟავების სახელების თანმიმდევრული ჩამოთვლით, N ბოლოდან დაწყებული; ამ შემთხვევაში, სუფიქსი "in" იცვლება სუფიქსით "il" ყველა ამინომჟავისთვის C ტერმინალურის გარდა. პეპტიდების სტრუქტურის აღსაწერად გამოიყენება არა ტრადიციული სტრუქტურული ფორმულები, არამედ აბრევიატურები, რათა აღნიშვნა უფრო კომპაქტური იყოს. H 2 N –CH–CONH –CH–CONH –CH 2–СONN –CH–COOH CH 2 SH CH 3 CH(CH 3)2 CH 2 OH პენტაპეპტიდი: ცისტეილალანილგლიცილვალილსერინი ან Cis-Ala-Gly-Val-Ser
პეპტიდური კავშირის ფორმირება ამინომჟავების ამინო და კარბოქსილის ჯგუფებს შეუძლიათ ურთიერთქმედება ერთმანეთთან ციკლის წარმოქმნის გარეშე: H 2 N –CH–COOH + H 2 N –CH–COOH CH 3 CH 2 OH H 2 N –CH–CO– NH –CH– COOH –H 2 O CH 3 CH 2 OH დიპეპტიდი ალანინი სერინი ალანილსერინი მიღებულ –CO–NH– კავშირს ეწოდება პეპტიდური ბმა, ხოლო ამინომჟავების ურთიერთქმედების პროდუქტს – პეპტიდი. თუ 2 ამინომჟავა რეაგირებს, მიიღება დიპეპტიდი; 3 ამინომჟავა - ტრიპეპტიდი და ა.შ. პეპტიდებს, რომელთა მოლეკულური წონა არ აღემატება 10000-ს, ეწოდება ოლიგოპეპტიდები, 10000-ზე მეტი მოლეკულური მასით - პოლიპეპტიდები, ანუ ცილები. პეპტიდების შემადგენლობაში არსებული პეპტიდური ბმები ქიმიური ბუნებით ამიდურია. პოლიპეპტიდური ჯაჭვი შედგება რეგულარულად განმეორებადი მონაკვეთებისგან, რომლებიც ქმნიან მოლეკულის ხერხემალს და ცვლადი სექციებისაგან - ამინომჟავების ნარჩენების გვერდითი რადიკალები. პოლიპეპტიდური ჯაჭვის დასაწყისი ითვლება დასასრულად, რომელსაც აქვს თავისუფალი ამინო ჯგუფი (N ბოლო), ხოლო პოლიპეპტიდური ჯაჭვი მთავრდება თავისუფალი კარბოქსილის ჯგუფით (C ბოლო). პეპტიდს ასახელებენ პეპტიდში შემავალი ამინომჟავების სახელების თანმიმდევრული ჩამოთვლით, N ბოლოდან დაწყებული; ამ შემთხვევაში, სუფიქსი "in" იცვლება სუფიქსით "il" ყველა ამინომჟავისთვის C ტერმინალურის გარდა. პეპტიდების სტრუქტურის აღსაწერად გამოიყენება არა ტრადიციული სტრუქტურული ფორმულები, არამედ აბრევიატურები, რათა აღნიშვნა უფრო კომპაქტური იყოს. H 2 N –CH–CONH –CH–CONH –CH 2–СONN –CH–COOH CH 2 SH CH 3 CH(CH 3)2 CH 2 OH პენტაპეპტიდი: ცისტეილალანილგლიცილვალილსერინი ან Cis-Ala-Gly-Val-Ser
 ცილები ამჟამად, ზოგადად მიღებულია ცილის მოლეკულის სტრუქტურის პოლიპეპტიდური თეორია. ცილები შეიძლება დაიყოს: – მოლეკულების ფორმის მიხედვით (გლობულური და ფიბრილარული); – მოლეკულური წონის მიხედვით (დაბალი და მაღალი მოლეკულური წონა); - შემადგენლობის ან ქიმიური სტრუქტურის მიხედვით (მარტივი და რთული); – შესრულებული ფუნქციების მიხედვით; – უჯრედში ლოკალიზაციით (ბირთვული, ციტოპლაზმური და ა.შ.); - ორგანიზმში ლოკალიზაციით (სისხლის ცილები, ღვიძლი და ა.შ.); - თუ ეს შესაძლებელია, ადაპტაციურად დაარეგულირეთ ამ ცილების რაოდენობა: ცილები, რომლებიც სინთეზირდება მუდმივი სიჩქარით (კონსტიტუციური) და ცილები, რომელთა სინთეზი შეიძლება გაიზარდოს გარემო ფაქტორების ზემოქმედებისას (ინდუქციური); – უჯრედში სიცოცხლის ხანგრძლივობით (ძალიან სწრაფად განახლებული ცილებიდან, ნახევარგამოყოფის პერიოდით 1 საათზე ნაკლები, ძალიან ნელა განახლებულ ცილებამდე, რომელთა ნახევარგამოყოფის პერიოდი გამოითვლება კვირებში და თვეებში); – პირველადი სტრუქტურისა და მასთან დაკავშირებული ფუნქციების მსგავსი სფეროების მიხედვით (ცილოვანი ოჯახები).
ცილები ამჟამად, ზოგადად მიღებულია ცილის მოლეკულის სტრუქტურის პოლიპეპტიდური თეორია. ცილები შეიძლება დაიყოს: – მოლეკულების ფორმის მიხედვით (გლობულური და ფიბრილარული); – მოლეკულური წონის მიხედვით (დაბალი და მაღალი მოლეკულური წონა); - შემადგენლობის ან ქიმიური სტრუქტურის მიხედვით (მარტივი და რთული); – შესრულებული ფუნქციების მიხედვით; – უჯრედში ლოკალიზაციით (ბირთვული, ციტოპლაზმური და ა.შ.); - ორგანიზმში ლოკალიზაციით (სისხლის ცილები, ღვიძლი და ა.შ.); - თუ ეს შესაძლებელია, ადაპტაციურად დაარეგულირეთ ამ ცილების რაოდენობა: ცილები, რომლებიც სინთეზირდება მუდმივი სიჩქარით (კონსტიტუციური) და ცილები, რომელთა სინთეზი შეიძლება გაიზარდოს გარემო ფაქტორების ზემოქმედებისას (ინდუქციური); – უჯრედში სიცოცხლის ხანგრძლივობით (ძალიან სწრაფად განახლებული ცილებიდან, ნახევარგამოყოფის პერიოდით 1 საათზე ნაკლები, ძალიან ნელა განახლებულ ცილებამდე, რომელთა ნახევარგამოყოფის პერიოდი გამოითვლება კვირებში და თვეებში); – პირველადი სტრუქტურისა და მასთან დაკავშირებული ფუნქციების მსგავსი სფეროების მიხედვით (ცილოვანი ოჯახები).
 ცილების ფუნქციები ცილების ფუნქცია კატალიზური (ფერმენტული) ტრანსპორტი სტრუქტურული (პლასტიკური) შეკუმშვა მარეგულირებელი (ჰორმონალური) დამცავი ენერგიის არსი მაგალითები ქიმიური რეაქციების დაჩქარება პეპსინი, ტრიპსინი, კატალაზა ორგანიზმში, ციტოქრომ ოქსიდაზა ტრანსპორტი (ტრანსპორტი) ჰემოგლობინი, ალბუმინი სხეულის ტრანსფერინი სიძლიერისა და კოლაგენის უზრუნველყოფა, ქსოვილის ელასტიურობა კერატინი კუნთების სარკომერების დამოკლება აქტინი, მიოზინი (შეკუმშვა) მეტაბოლიზმის რეგულირება ინსულინში, სომატოტროპინში, უჯრედებსა და ქსოვილებში გლუკაგონი, კორტიკოტრანსპინი ორგანიზმის დაცვა ინტერფერონებისგან, დამაზიანებელი ფაქტორებისგან იმუნოგლობულინები, რემბინინოგენაზა ენერგია საკვების ცილების და ამინომჟავების ქსოვილის დაშლის გამო
ცილების ფუნქციები ცილების ფუნქცია კატალიზური (ფერმენტული) ტრანსპორტი სტრუქტურული (პლასტიკური) შეკუმშვა მარეგულირებელი (ჰორმონალური) დამცავი ენერგიის არსი მაგალითები ქიმიური რეაქციების დაჩქარება პეპსინი, ტრიპსინი, კატალაზა ორგანიზმში, ციტოქრომ ოქსიდაზა ტრანსპორტი (ტრანსპორტი) ჰემოგლობინი, ალბუმინი სხეულის ტრანსფერინი სიძლიერისა და კოლაგენის უზრუნველყოფა, ქსოვილის ელასტიურობა კერატინი კუნთების სარკომერების დამოკლება აქტინი, მიოზინი (შეკუმშვა) მეტაბოლიზმის რეგულირება ინსულინში, სომატოტროპინში, უჯრედებსა და ქსოვილებში გლუკაგონი, კორტიკოტრანსპინი ორგანიზმის დაცვა ინტერფერონებისგან, დამაზიანებელი ფაქტორებისგან იმუნოგლობულინები, რემბინინოგენაზა ენერგია საკვების ცილების და ამინომჟავების ქსოვილის დაშლის გამო
 მარტივი ცილების კლასიფიკაცია ალბუმინი. შრატის ცილების ოსმოსური წნევის დაახლოებით 75-80% მოდის ალბუმინზე; კიდევ ერთი ფუნქციაა ცხიმოვანი მჟავების ტრანსპორტირება. გლობულინები სისხლში გვხვდება ბილირუბინთან და მაღალი სიმკვრივის ლიპოპროტეინებთან ერთად. β გლობულინის ფრაქცია მოიცავს პროთრომბინს, რომელიც არის თრომბინის წინამორბედი, ცილა, რომელიც პასუხისმგებელია სისხლის შედედების დროს სისხლის ფიბრინოგენის ფიბრინად გადაქცევაზე. გლობულინები ასრულებენ დამცავ ფუნქციას. პროტამინები არის დაბალი მოლეკულური წონის ცილები, რომლებსაც აქვთ გამოხატული ძირითადი თვისებები მათ შემადგენლობაში 60-დან 85% არგინინის არსებობის გამო. უჯრედის ბირთვებში ისინი დაკავშირებულია დნმ-თან. ჰისტონები ასევე მცირე ძირითადი ცილებია. ისინი შეიცავს ლიზინს და არგინინს (20-30%). ჰისტონები მნიშვნელოვან როლს ასრულებენ გენის ექსპრესიის რეგულირებაში. პროლამინი მცენარეული წარმოშობის ცილებია, რომლებიც ძირითადად მარცვლეულის თესლებში გვხვდება. ამ ჯგუფის ყველა ცილა იძლევა მნიშვნელოვან რაოდენობას პროლინს ჰიდროლიზის დროს. პროლამინები შეიცავს 20-25% გლუტამინის მჟავას და 10-15% პროლინს. ყველაზე შესწავლილი არის ორიზენინი (ბრინჯისგან), გლუტენინი (ხორბლისგან), ზეინი (სიმინდისგან) და სხვა გლუტელინები არის მარტივი ცილები, რომლებიც გვხვდება მარცვლეულის თესლში და მცენარეების მწვანე ნაწილებში. გლუტელინებს ახასიათებთ გლუტამინის მჟავის შედარებით მაღალი შემცველობა და ლიზინის არსებობა. გლუტელინები არის შესანახი ცილები.
მარტივი ცილების კლასიფიკაცია ალბუმინი. შრატის ცილების ოსმოსური წნევის დაახლოებით 75-80% მოდის ალბუმინზე; კიდევ ერთი ფუნქციაა ცხიმოვანი მჟავების ტრანსპორტირება. გლობულინები სისხლში გვხვდება ბილირუბინთან და მაღალი სიმკვრივის ლიპოპროტეინებთან ერთად. β გლობულინის ფრაქცია მოიცავს პროთრომბინს, რომელიც არის თრომბინის წინამორბედი, ცილა, რომელიც პასუხისმგებელია სისხლის შედედების დროს სისხლის ფიბრინოგენის ფიბრინად გადაქცევაზე. გლობულინები ასრულებენ დამცავ ფუნქციას. პროტამინები არის დაბალი მოლეკულური წონის ცილები, რომლებსაც აქვთ გამოხატული ძირითადი თვისებები მათ შემადგენლობაში 60-დან 85% არგინინის არსებობის გამო. უჯრედის ბირთვებში ისინი დაკავშირებულია დნმ-თან. ჰისტონები ასევე მცირე ძირითადი ცილებია. ისინი შეიცავს ლიზინს და არგინინს (20-30%). ჰისტონები მნიშვნელოვან როლს ასრულებენ გენის ექსპრესიის რეგულირებაში. პროლამინი მცენარეული წარმოშობის ცილებია, რომლებიც ძირითადად მარცვლეულის თესლებში გვხვდება. ამ ჯგუფის ყველა ცილა იძლევა მნიშვნელოვან რაოდენობას პროლინს ჰიდროლიზის დროს. პროლამინები შეიცავს 20-25% გლუტამინის მჟავას და 10-15% პროლინს. ყველაზე შესწავლილი არის ორიზენინი (ბრინჯისგან), გლუტენინი (ხორბლისგან), ზეინი (სიმინდისგან) და სხვა გლუტელინები არის მარტივი ცილები, რომლებიც გვხვდება მარცვლეულის თესლში და მცენარეების მწვანე ნაწილებში. გლუტელინებს ახასიათებთ გლუტამინის მჟავის შედარებით მაღალი შემცველობა და ლიზინის არსებობა. გლუტელინები არის შესანახი ცილები.
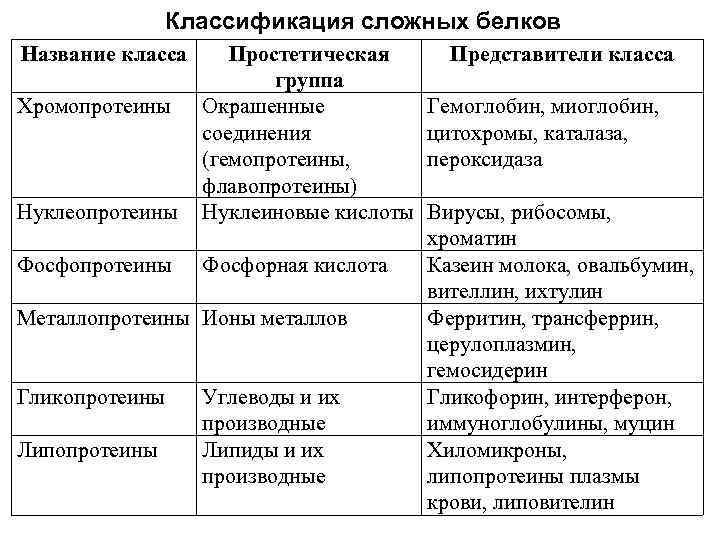 კომპლექსური ცილების კლასიფიკაცია კლასის დასახელება ნუკლეოპროტეინები პროთეზური ჯგუფი ფერადი ნაერთები (ჰემოპროტეინები, ფლავოპროტეინები) ნუკლეინის მჟავები ფოსფოპროტეინები ფოსფორის მჟავა ქრომოპროტეინები მეტალოპროტეინები მეტალის იონები გლიკოპროტეინები ლიპოპროტეინები ნახშირწყლები და მათი წარმოებულები ლიპიდები, ჰემოგლობინის წარმოებულები და მათი წარმოებულები es, კატალაზა, რიბო პეროქსიდაზა სომა ქრომატინი რძის კაზეინი, ოვალბუმინი, ვიტელინი, იხტულინი ფერიტინი, ტრანსფერინი, ცერულოპლაზმინი, ჰემოსიდერინი გლიკოფორინი, ინტერფერონი, იმუნოგლობულინები, მუცინი ქილომიკრონები, სისხლის პლაზმის ლიპოპროტეინები, ლიპოვიტელინი
კომპლექსური ცილების კლასიფიკაცია კლასის დასახელება ნუკლეოპროტეინები პროთეზური ჯგუფი ფერადი ნაერთები (ჰემოპროტეინები, ფლავოპროტეინები) ნუკლეინის მჟავები ფოსფოპროტეინები ფოსფორის მჟავა ქრომოპროტეინები მეტალოპროტეინები მეტალის იონები გლიკოპროტეინები ლიპოპროტეინები ნახშირწყლები და მათი წარმოებულები ლიპიდები, ჰემოგლობინის წარმოებულები და მათი წარმოებულები es, კატალაზა, რიბო პეროქსიდაზა სომა ქრომატინი რძის კაზეინი, ოვალბუმინი, ვიტელინი, იხტულინი ფერიტინი, ტრანსფერინი, ცერულოპლაზმინი, ჰემოსიდერინი გლიკოფორინი, ინტერფერონი, იმუნოგლობულინები, მუცინი ქილომიკრონები, სისხლის პლაზმის ლიპოპროტეინები, ლიპოვიტელინი
 ცილის პირველადი სტრუქტურა ცილის პირველადი სტრუქტურა არის ამინომჟავების თანმიმდევრობა პოლიპეპტიდურ ჯაჭვში. იგი განისაზღვრება ცილიდან ამინომჟავების თანმიმდევრული მოცილებით ჰიდროლიზით. N ტერმინალური ამინომჟავის მოსაშორებლად ცილა მუშავდება 2, 4 დინიტროფტორბენზოლით და მჟავა ჰიდროლიზის შემდეგ მხოლოდ ერთი N ტერმინალური მჟავა უკავშირდება ამ რეაგენტს (სანგერის მეთოდი). ედმანის მეთოდის მიხედვით N ტერმინალური მჟავა გამოიყოფა ჰიდროლიზის დროს რეაქციის პროდუქტის სახით ფენილ იზოთიოციანატთან. C ტერმინალური მჟავის დასადგენად, ჰიდროლიზი ჩვეულებრივ გამოიყენება სპეციალური ფერმენტის კარბოქსიპეპტიდაზას თანდასწრებით, რომელიც არღვევს პეპტიდურ კავშირს პეპტიდის ბოლოდან, რომელიც შეიცავს თავისუფალ კარბოქსილის ჯგუფს. ასევე არსებობს C ტერმინალური მჟავის მოცილების ქიმიური მეთოდები, მაგალითად, ჰიდრაზინის გამოყენებით (აკაბორის მეთოდი).
ცილის პირველადი სტრუქტურა ცილის პირველადი სტრუქტურა არის ამინომჟავების თანმიმდევრობა პოლიპეპტიდურ ჯაჭვში. იგი განისაზღვრება ცილიდან ამინომჟავების თანმიმდევრული მოცილებით ჰიდროლიზით. N ტერმინალური ამინომჟავის მოსაშორებლად ცილა მუშავდება 2, 4 დინიტროფტორბენზოლით და მჟავა ჰიდროლიზის შემდეგ მხოლოდ ერთი N ტერმინალური მჟავა უკავშირდება ამ რეაგენტს (სანგერის მეთოდი). ედმანის მეთოდის მიხედვით N ტერმინალური მჟავა გამოიყოფა ჰიდროლიზის დროს რეაქციის პროდუქტის სახით ფენილ იზოთიოციანატთან. C ტერმინალური მჟავის დასადგენად, ჰიდროლიზი ჩვეულებრივ გამოიყენება სპეციალური ფერმენტის კარბოქსიპეპტიდაზას თანდასწრებით, რომელიც არღვევს პეპტიდურ კავშირს პეპტიდის ბოლოდან, რომელიც შეიცავს თავისუფალ კარბოქსილის ჯგუფს. ასევე არსებობს C ტერმინალური მჟავის მოცილების ქიმიური მეთოდები, მაგალითად, ჰიდრაზინის გამოყენებით (აკაბორის მეთოდი).
 ცილის მეორადი სტრუქტურა არის ძალიან გრძელი პოლიპეპტიდური ჯაჭვის ხვეული ან დაკეცილი კონფორმაციით შეფუთვის მეთოდი. სპირალის ან ნაკეცის მოხვევები ერთმანეთთან ძირითადად იმართება ინტრამოლეკულური ბმებით, რომლებიც წარმოიქმნება სპირალის ან ნაკეცის ერთი მობრუნების წყალბადის ატომს (–NH ან –COOH ჯგუფებში) და მიმდებარე მდებარე ელექტროუარყოფით ატომს (ჟანგბადი ან აზოტი). შემობრუნება ან დაკეცვა.
ცილის მეორადი სტრუქტურა არის ძალიან გრძელი პოლიპეპტიდური ჯაჭვის ხვეული ან დაკეცილი კონფორმაციით შეფუთვის მეთოდი. სპირალის ან ნაკეცის მოხვევები ერთმანეთთან ძირითადად იმართება ინტრამოლეკულური ბმებით, რომლებიც წარმოიქმნება სპირალის ან ნაკეცის ერთი მობრუნების წყალბადის ატომს (–NH ან –COOH ჯგუფებში) და მიმდებარე მდებარე ელექტროუარყოფით ატომს (ჟანგბადი ან აზოტი). შემობრუნება ან დაკეცვა.
 ცილის მესამეული სტრუქტურა ცილის მესამეული სტრუქტურა არის პოლიპეპტიდური სპირალის ან დაკეცილი სტრუქტურის სამგანზომილებიანი სივრცითი ორიენტაცია გარკვეულ მოცულობაში. არსებობს სფერული (სფერული) და ფიბრილარული (მოგრძო, ბოჭკოვანი) მესამეული სტრუქტურები. მესამეული სტრუქტურა იქმნება ავტომატურად, სპონტანურად და მთლიანად განისაზღვრება ცილის პირველადი სტრუქტურით. ამ შემთხვევაში, ამინომჟავების ნარჩენების გვერდითი რადიკალები ურთიერთქმედებენ. მესამეული სტრუქტურის სტაბილიზაცია ხორციელდება ამინომჟავის რადიკალებს შორის წყალბადის, იონური, დისულფიდური ბმების წარმოქმნის გამო, აგრეთვე ვან დერ ვაალის მიზიდულობის ძალების გამო არაპოლარული ნახშირწყალბადის რადიკალებს შორის.
ცილის მესამეული სტრუქტურა ცილის მესამეული სტრუქტურა არის პოლიპეპტიდური სპირალის ან დაკეცილი სტრუქტურის სამგანზომილებიანი სივრცითი ორიენტაცია გარკვეულ მოცულობაში. არსებობს სფერული (სფერული) და ფიბრილარული (მოგრძო, ბოჭკოვანი) მესამეული სტრუქტურები. მესამეული სტრუქტურა იქმნება ავტომატურად, სპონტანურად და მთლიანად განისაზღვრება ცილის პირველადი სტრუქტურით. ამ შემთხვევაში, ამინომჟავების ნარჩენების გვერდითი რადიკალები ურთიერთქმედებენ. მესამეული სტრუქტურის სტაბილიზაცია ხორციელდება ამინომჟავის რადიკალებს შორის წყალბადის, იონური, დისულფიდური ბმების წარმოქმნის გამო, აგრეთვე ვან დერ ვაალის მიზიდულობის ძალების გამო არაპოლარული ნახშირწყალბადის რადიკალებს შორის.
 ამინომჟავის რადიკალებს შორის ობლიგაციების ფორმირების სქემა 1 – იონური ბმები, 2 – წყალბადის ბმები, 3 – ჰიდროფობიური ურთიერთქმედება, 4 – დისულფიდური ბმები.
ამინომჟავის რადიკალებს შორის ობლიგაციების ფორმირების სქემა 1 – იონური ბმები, 2 – წყალბადის ბმები, 3 – ჰიდროფობიური ურთიერთქმედება, 4 – დისულფიდური ბმები.
 ცილის მეოთხეული სტრუქტურა ცილის მეოთხეული სტრუქტურა წარმოადგენს სივრცეში ცალკეული პოლიპეპტიდური ჯაჭვების განლაგებისა და სტრუქტურულად და ფუნქციურად ერთიანი მაკრომოლეკულური წარმონაქმნის ფორმირების გზას. მიღებულ მოლეკულას ეწოდება ოლიგომერი, ხოლო ცალკეულ პოლიპეპტიდურ ჯაჭვებს, რომელთაგანაც იგი შედგება, ეწოდება პროტომერები, მონომერები ან ქვედანაყოფები (ჩვეულებრივ ლუწი რიცხვი: 2, 4, ნაკლებად ხშირად 6 ან 8). მაგალითად, ჰემოგლობინის მოლეკულა შედგება ორი და ორი პოლიპეპტიდური ჯაჭვისგან. თითოეული პოლიპეპტიდური ჯაჭვი აკრავს ჰემის ჯგუფს, არაცილოვან პიგმენტს, რომელიც სისხლს წითელ ფერს აძლევს. სწორედ ჰემის შემადგენლობაში არის რკინის კატიონი, რომელსაც შეუძლია სხეულის ფუნქციონირებისთვის საჭირო ჟანგბადის მიმაგრება და მთელ სხეულში გადატანა. ჰემოგლობინის ტეტრამერი ცილების დაახლოებით 5%-ს აქვს მეოთხეული სტრუქტურა, მათ შორის ჰემოგლობინი, იმუნოგლობულინები, ინსულინი, ფერიტინი და თითქმის ყველა დნმ და რნმ პოლიმერაზა. ინსულინის ჰექსამერი
ცილის მეოთხეული სტრუქტურა ცილის მეოთხეული სტრუქტურა წარმოადგენს სივრცეში ცალკეული პოლიპეპტიდური ჯაჭვების განლაგებისა და სტრუქტურულად და ფუნქციურად ერთიანი მაკრომოლეკულური წარმონაქმნის ფორმირების გზას. მიღებულ მოლეკულას ეწოდება ოლიგომერი, ხოლო ცალკეულ პოლიპეპტიდურ ჯაჭვებს, რომელთაგანაც იგი შედგება, ეწოდება პროტომერები, მონომერები ან ქვედანაყოფები (ჩვეულებრივ ლუწი რიცხვი: 2, 4, ნაკლებად ხშირად 6 ან 8). მაგალითად, ჰემოგლობინის მოლეკულა შედგება ორი და ორი პოლიპეპტიდური ჯაჭვისგან. თითოეული პოლიპეპტიდური ჯაჭვი აკრავს ჰემის ჯგუფს, არაცილოვან პიგმენტს, რომელიც სისხლს წითელ ფერს აძლევს. სწორედ ჰემის შემადგენლობაში არის რკინის კატიონი, რომელსაც შეუძლია სხეულის ფუნქციონირებისთვის საჭირო ჟანგბადის მიმაგრება და მთელ სხეულში გადატანა. ჰემოგლობინის ტეტრამერი ცილების დაახლოებით 5%-ს აქვს მეოთხეული სტრუქტურა, მათ შორის ჰემოგლობინი, იმუნოგლობულინები, ინსულინი, ფერიტინი და თითქმის ყველა დნმ და რნმ პოლიმერაზა. ინსულინის ჰექსამერი
 ფერთა რეაქციები ცილების და ამინომჟავების გამოსავლენად პეპტიდების, ცილების და ცალკეული ამინომჟავების იდენტიფიცირებისთვის გამოიყენება ე.წ. „ფერადი რეაქციები“. უნივერსალური რეაქცია პეპტიდურ ჯგუფზე არის წითელ-იისფერი ფერის გამოჩენა, როდესაც სპილენძის (II) იონები ემატება ცილის ხსნარს ტუტე გარემოში (ბიურეტის რეაქცია). რეაქცია არომატულ ამინომჟავების ნარჩენებზე - ტიროზინზე და ფენილალანინზე - ყვითელი ფერის გამოჩენა ცილის ხსნარის კონცენტრირებული აზოტის მჟავით დამუშავებისას (ქსანტოპროტეინის რეაქცია). გოგირდის შემცველი ცილები იღებენ შავ ფერს ტყვიის(II) აცეტატის ხსნარით ტუტე გარემოში გაცხელებისას (ფოლის რეაქცია). ამინომჟავების ზოგადი თვისებრივი რეაქცია არის ლურჯი-იისფერი ფერის ფორმირება ნინჰიდრინთან ურთიერთობისას. პროტეინები ასევე იძლევა ნინჰიდრინის რეაქციას.
ფერთა რეაქციები ცილების და ამინომჟავების გამოსავლენად პეპტიდების, ცილების და ცალკეული ამინომჟავების იდენტიფიცირებისთვის გამოიყენება ე.წ. „ფერადი რეაქციები“. უნივერსალური რეაქცია პეპტიდურ ჯგუფზე არის წითელ-იისფერი ფერის გამოჩენა, როდესაც სპილენძის (II) იონები ემატება ცილის ხსნარს ტუტე გარემოში (ბიურეტის რეაქცია). რეაქცია არომატულ ამინომჟავების ნარჩენებზე - ტიროზინზე და ფენილალანინზე - ყვითელი ფერის გამოჩენა ცილის ხსნარის კონცენტრირებული აზოტის მჟავით დამუშავებისას (ქსანტოპროტეინის რეაქცია). გოგირდის შემცველი ცილები იღებენ შავ ფერს ტყვიის(II) აცეტატის ხსნარით ტუტე გარემოში გაცხელებისას (ფოლის რეაქცია). ამინომჟავების ზოგადი თვისებრივი რეაქცია არის ლურჯი-იისფერი ფერის ფორმირება ნინჰიდრინთან ურთიერთობისას. პროტეინები ასევე იძლევა ნინჰიდრინის რეაქციას.
 ცილების და პეპტიდების მნიშვნელობა ცილები წარმოადგენს უჯრედის ქიმიური აქტივობის მატერიალურ საფუძველს. ბუნებაში ცილების ფუნქციები უნივერსალურია. მათ შორის არის ფერმენტები, ჰორმონები, სტრუქტურული (კერატინი, ფიბროინი, კოლაგენი), სატრანსპორტო (ჰემოგლობინი, მიოგლობინი), საავტომობილო (აქტინი, მიოზინი), დამცავი (იმუნოგლობულინები), შესანახი ცილები (კაზეინი, კვერცხის ალბუმინი), ტოქსინები (გველის შხამი, დიფტერიის ტოქსინი). ბიოლოგიური თვალსაზრისით, პეპტიდები განსხვავდება ცილებისგან ფუნქციების უფრო ვიწრო დიაპაზონში. პეპტიდების ყველაზე ტიპიური მარეგულირებელი ფუნქცია (ჰორმონები, ანტიბიოტიკები, ტოქსინები, ფერმენტების ინჰიბიტორები და აქტივატორები, მემბრანების მეშვეობით იონური გადამტანები და ა.შ.). ახლახან აღმოაჩინეს ტვინის პეპტიდების ჯგუფი - ნეიროპეპტიდები. ისინი გავლენას ახდენენ სწავლისა და მეხსიერების პროცესებზე, არეგულირებენ ძილს და აქვთ ტკივილგამაყუჩებელი ფუნქცია; არსებობს კავშირი ზოგიერთ ნეიროფსიქიატრიულ დაავადებას, როგორიცაა შიზოფრენია და თავის ტვინში გარკვეული პეპტიდების შემცველობას შორის. ამჟამად მიღწეულია პროგრესი ცილების სტრუქტურასა და ფუნქციებს შორის ურთიერთობის პრობლემის შესწავლაში, სხეულის ცხოვრების უმნიშვნელოვანეს პროცესებში მათი მონაწილეობის მექანიზმისა და მრავალი დაავადების პათოგენეზის მოლეკულური საფუძვლის გაგებაში. აქტუალური პრობლემები მოიცავს ცილის ქიმიურ სინთეზს. ბუნებრივი პეპტიდების და ცილების ანალოგების სინთეზური წარმოება მიზნად ისახავს ისეთი საკითხების გადაჭრას, როგორიცაა უჯრედებში ამ ნაერთების მოქმედების მექანიზმის გარკვევა, მათ აქტივობასა და სივრცულ სტრუქტურას შორის კავშირის დამყარება, ახალი მედიკამენტებისა და საკვები პროდუქტების შექმნა და ასევე საშუალებას გვაძლევს მივუდგეთ ორგანიზმში მიმდინარე პროცესების მოდელირებას.
ცილების და პეპტიდების მნიშვნელობა ცილები წარმოადგენს უჯრედის ქიმიური აქტივობის მატერიალურ საფუძველს. ბუნებაში ცილების ფუნქციები უნივერსალურია. მათ შორის არის ფერმენტები, ჰორმონები, სტრუქტურული (კერატინი, ფიბროინი, კოლაგენი), სატრანსპორტო (ჰემოგლობინი, მიოგლობინი), საავტომობილო (აქტინი, მიოზინი), დამცავი (იმუნოგლობულინები), შესანახი ცილები (კაზეინი, კვერცხის ალბუმინი), ტოქსინები (გველის შხამი, დიფტერიის ტოქსინი). ბიოლოგიური თვალსაზრისით, პეპტიდები განსხვავდება ცილებისგან ფუნქციების უფრო ვიწრო დიაპაზონში. პეპტიდების ყველაზე ტიპიური მარეგულირებელი ფუნქცია (ჰორმონები, ანტიბიოტიკები, ტოქსინები, ფერმენტების ინჰიბიტორები და აქტივატორები, მემბრანების მეშვეობით იონური გადამტანები და ა.შ.). ახლახან აღმოაჩინეს ტვინის პეპტიდების ჯგუფი - ნეიროპეპტიდები. ისინი გავლენას ახდენენ სწავლისა და მეხსიერების პროცესებზე, არეგულირებენ ძილს და აქვთ ტკივილგამაყუჩებელი ფუნქცია; არსებობს კავშირი ზოგიერთ ნეიროფსიქიატრიულ დაავადებას, როგორიცაა შიზოფრენია და თავის ტვინში გარკვეული პეპტიდების შემცველობას შორის. ამჟამად მიღწეულია პროგრესი ცილების სტრუქტურასა და ფუნქციებს შორის ურთიერთობის პრობლემის შესწავლაში, სხეულის ცხოვრების უმნიშვნელოვანეს პროცესებში მათი მონაწილეობის მექანიზმისა და მრავალი დაავადების პათოგენეზის მოლეკულური საფუძვლის გაგებაში. აქტუალური პრობლემები მოიცავს ცილის ქიმიურ სინთეზს. ბუნებრივი პეპტიდების და ცილების ანალოგების სინთეზური წარმოება მიზნად ისახავს ისეთი საკითხების გადაჭრას, როგორიცაა უჯრედებში ამ ნაერთების მოქმედების მექანიზმის გარკვევა, მათ აქტივობასა და სივრცულ სტრუქტურას შორის კავშირის დამყარება, ახალი მედიკამენტებისა და საკვები პროდუქტების შექმნა და ასევე საშუალებას გვაძლევს მივუდგეთ ორგანიზმში მიმდინარე პროცესების მოდელირებას.
 რაღაც საინტერესო ცილების შესახებ ცილები არის სხვადასხვა სახის ბიოლოგიური წებოების საფუძველი. ამრიგად, ობობების სანადირო ქსელები ძირითადად შედგება ფიბროინისგან, ცილისგან, რომელიც გამოიყოფა არაქნოიდული მეჭეჭებით. ეს სიროფი, ბლანტი ნივთიერება ჰაერში მკვრივდება, ძლიერ, წყალში უხსნად ძაფად. აბრეშუმი, რომელიც ქმნის ქსელის სპირალურ ძაფს, შეიცავს წებოს, რომელიც ინახავს მტაცებელს. თავად ობობა თავისუფლად ეშვება რადიალური ძაფების გასწვრივ. სპეციალური წებოების წყალობით ბუზებს და სხვა მწერებს შეუძლიათ აკრობატიკის უბრალოდ სასწაულების მოხდენა. პეპლები კვერცხებს მცენარის ფოთლებს აწებებენ, სვიფტების ზოგიერთი სახეობა ბუდეებს აშენებს სანერწყვე ჯირკვლების გამაგრებული სეკრეციისგან, ზუთხები კვერცხებს ქვედა ქვებზე ამაგრებენ. ზამთრისთვის ან გვალვის პერიოდში ლოკოკინების ზოგიერთი სახეობა თავის ჭურვებს აძლევს სპეციალურ „კარს“, რომელსაც თავად ლოკოკინა აგებს წებოვანი, გამაგრებული ცილისგან, რომელიც შეიცავს ცაცხვს. გარე სამყაროსგან საკმაოდ მყარი ბარიერით შემოღობილი ლოკოკინა თავის ნაჭუჭში არახელსაყრელ დროს ელის. როდესაც სიტუაცია იცვლება, ის უბრალოდ ჭამს მას და წყვეტს ცხოვრებას, როგორც თავშესაფარი. წყალქვეშა მაცხოვრებლების მიერ გამოყენებული წებოები უნდა გამკვრივდეს წყლის ქვეშ. აქედან გამომდინარე, ისინი შეიცავენ რამდენიმე განსხვავებულ ცილას, რომლებიც მოგერიებენ წყალს და ურთიერთქმედებენ ერთმანეთთან ძლიერი წებოს შესაქმნელად. წებო, რომელიც მიდიებს ქვას ამაგრებს, წყალში უხსნადია და ეპოქსიდური ფისიზე ორჯერ ძლიერია. ახლა ისინი ცდილობენ ამ ცილის სინთეზირებას ლაბორატორიაში. ადჰეზივების უმეტესობა არ მოითმენს ტენიანობას, მაგრამ მიდიის ცილის წებო შეიძლება გამოყენებულ იქნას ძვლებისა და კბილების ერთმანეთთან დასამაგრებლად. ეს ცილა არ იწვევს ორგანიზმის უარყოფას, რაც ძალიან მნიშვნელოვანია მედიკამენტებისთვის.
რაღაც საინტერესო ცილების შესახებ ცილები არის სხვადასხვა სახის ბიოლოგიური წებოების საფუძველი. ამრიგად, ობობების სანადირო ქსელები ძირითადად შედგება ფიბროინისგან, ცილისგან, რომელიც გამოიყოფა არაქნოიდული მეჭეჭებით. ეს სიროფი, ბლანტი ნივთიერება ჰაერში მკვრივდება, ძლიერ, წყალში უხსნად ძაფად. აბრეშუმი, რომელიც ქმნის ქსელის სპირალურ ძაფს, შეიცავს წებოს, რომელიც ინახავს მტაცებელს. თავად ობობა თავისუფლად ეშვება რადიალური ძაფების გასწვრივ. სპეციალური წებოების წყალობით ბუზებს და სხვა მწერებს შეუძლიათ აკრობატიკის უბრალოდ სასწაულების მოხდენა. პეპლები კვერცხებს მცენარის ფოთლებს აწებებენ, სვიფტების ზოგიერთი სახეობა ბუდეებს აშენებს სანერწყვე ჯირკვლების გამაგრებული სეკრეციისგან, ზუთხები კვერცხებს ქვედა ქვებზე ამაგრებენ. ზამთრისთვის ან გვალვის პერიოდში ლოკოკინების ზოგიერთი სახეობა თავის ჭურვებს აძლევს სპეციალურ „კარს“, რომელსაც თავად ლოკოკინა აგებს წებოვანი, გამაგრებული ცილისგან, რომელიც შეიცავს ცაცხვს. გარე სამყაროსგან საკმაოდ მყარი ბარიერით შემოღობილი ლოკოკინა თავის ნაჭუჭში არახელსაყრელ დროს ელის. როდესაც სიტუაცია იცვლება, ის უბრალოდ ჭამს მას და წყვეტს ცხოვრებას, როგორც თავშესაფარი. წყალქვეშა მაცხოვრებლების მიერ გამოყენებული წებოები უნდა გამკვრივდეს წყლის ქვეშ. აქედან გამომდინარე, ისინი შეიცავენ რამდენიმე განსხვავებულ ცილას, რომლებიც მოგერიებენ წყალს და ურთიერთქმედებენ ერთმანეთთან ძლიერი წებოს შესაქმნელად. წებო, რომელიც მიდიებს ქვას ამაგრებს, წყალში უხსნადია და ეპოქსიდური ფისიზე ორჯერ ძლიერია. ახლა ისინი ცდილობენ ამ ცილის სინთეზირებას ლაბორატორიაში. ადჰეზივების უმეტესობა არ მოითმენს ტენიანობას, მაგრამ მიდიის ცილის წებო შეიძლება გამოყენებულ იქნას ძვლებისა და კბილების ერთმანეთთან დასამაგრებლად. ეს ცილა არ იწვევს ორგანიზმის უარყოფას, რაც ძალიან მნიშვნელოვანია მედიკამენტებისთვის.
 რაღაც საინტერესო ცილების შესახებ L ასპარტილ L ფენილალანინის მეთილის ეთერს აქვს ძალიან ტკბილი გემო. CH3 OOC-CH(CH2C6H5)-NH-CO-CH(NH2)-CH2-COOH. ნივთიერება ცნობილია სავაჭრო სახელწოდებით "ასპარტამი". ასპარტამი არა მხოლოდ შაქარზე ტკბილია (100-150-ჯერ), არამედ აძლიერებს მის ტკბილ გემოს, განსაკუთრებით ლიმონმჟავას თანდასწრებით. ასპარტამის მრავალი წარმოებული ასევე ტკბილია. 1895 წელს ნიგერიის ველურ ბუნებაში აღმოჩენილი Dioscoreophylum cumminsii (რუსული სახელის გარეშე) მარცვლებიდან გამოიყო ცილა მონელინი, რომელიც შაქარზე 1500-2000-ჯერ ტკბილია. სხვა აფრიკული მცენარის, Thaumatococcus daniellii-ის კაშკაშა წითელი ხორციანი ნაყოფისგან გამოყოფილი ცილა თაუმატინი კიდევ უფრო ძლიერად აჭარბებდა საქაროზას - 4000-ჯერ. თაუმატინის ტკბილი გემოს ინტენსივობა კიდევ უფრო იზრდება, როდესაც ეს ცილა ურთიერთქმედებს ალუმინის იონებთან. შედეგად მიღებული კომპლექსი, რომელმაც მიიღო სავაჭრო სახელი ტალინი, 35000-ჯერ უფრო ტკბილია ვიდრე საქაროზა; თუ შევადარებთ არა ტალინისა და საქაროზის მასებს, არამედ მათი მოლეკულების რაოდენობას, მაშინ ტალინი 200 ათასჯერ უფრო ტკბილი აღმოჩნდება! კიდევ ერთი ძალიან ტკბილი ცილა, მირაკულინი, იზოლირებული იქნა გასულ საუკუნეში ბუჩქის Synsepalum dulcificum daniellii-ს წითელი ნაყოფიდან, რომელსაც "სასწაულებრივი" უწოდეს: იცვლება ადამიანის გემო შეგრძნებები, ვინც ამ ხილს ღეჭავს. ამგვარად, ძმარი ავითარებს სასიამოვნო ღვინის გემოს, ლიმონის წვენი იქცევა ტკბილ სასმელად და ეფექტი დიდხანს გრძელდება. თუ ყველა ეს ეგზოტიკური ხილი ოდესმე გაშენდება პლანტაციებზე, შაქრის ინდუსტრიას გაცილებით ნაკლები პრობლემა ექნება პროდუქციის ტრანსპორტირებასთან დაკავშირებით. ყოველივე ამის შემდეგ, თაუმატინის პატარა ნაჭერს შეუძლია შეცვალოს გრანულირებული შაქრის მთელი ტომარა! 70-იანი წლების დასაწყისში სინთეზირებული იყო ნაერთი, ყველაზე ტკბილი ყველა სინთეზირებული. ეს არის დიპეპტიდი, რომელიც აგებულია ორი ამინომჟავის - ასპარტისა და ამინომალონის ნარჩენებისგან. დიპეპტიდში ამინომალონური მჟავის ნარჩენების ორი კარბოქსილის ჯგუფი ჩანაცვლებულია მეთანოლითა და ფენქოლით წარმოქმნილი ეთერული ჯგუფებით (ის გვხვდება მცენარეთა ეთერზეთებში და გამოიყოფა ტურპენტინისგან). ეს ნივთიერება დაახლოებით 33000-ჯერ უფრო ტკბილია ვიდრე საქაროზა. იმისათვის, რომ შოკოლადის ფილა ჩვეულებრივად ტკბილი გახდეს, საკმარისია ამ სანელებლის მილიგრამის ფრაქცია.
რაღაც საინტერესო ცილების შესახებ L ასპარტილ L ფენილალანინის მეთილის ეთერს აქვს ძალიან ტკბილი გემო. CH3 OOC-CH(CH2C6H5)-NH-CO-CH(NH2)-CH2-COOH. ნივთიერება ცნობილია სავაჭრო სახელწოდებით "ასპარტამი". ასპარტამი არა მხოლოდ შაქარზე ტკბილია (100-150-ჯერ), არამედ აძლიერებს მის ტკბილ გემოს, განსაკუთრებით ლიმონმჟავას თანდასწრებით. ასპარტამის მრავალი წარმოებული ასევე ტკბილია. 1895 წელს ნიგერიის ველურ ბუნებაში აღმოჩენილი Dioscoreophylum cumminsii (რუსული სახელის გარეშე) მარცვლებიდან გამოიყო ცილა მონელინი, რომელიც შაქარზე 1500-2000-ჯერ ტკბილია. სხვა აფრიკული მცენარის, Thaumatococcus daniellii-ის კაშკაშა წითელი ხორციანი ნაყოფისგან გამოყოფილი ცილა თაუმატინი კიდევ უფრო ძლიერად აჭარბებდა საქაროზას - 4000-ჯერ. თაუმატინის ტკბილი გემოს ინტენსივობა კიდევ უფრო იზრდება, როდესაც ეს ცილა ურთიერთქმედებს ალუმინის იონებთან. შედეგად მიღებული კომპლექსი, რომელმაც მიიღო სავაჭრო სახელი ტალინი, 35000-ჯერ უფრო ტკბილია ვიდრე საქაროზა; თუ შევადარებთ არა ტალინისა და საქაროზის მასებს, არამედ მათი მოლეკულების რაოდენობას, მაშინ ტალინი 200 ათასჯერ უფრო ტკბილი აღმოჩნდება! კიდევ ერთი ძალიან ტკბილი ცილა, მირაკულინი, იზოლირებული იქნა გასულ საუკუნეში ბუჩქის Synsepalum dulcificum daniellii-ს წითელი ნაყოფიდან, რომელსაც "სასწაულებრივი" უწოდეს: იცვლება ადამიანის გემო შეგრძნებები, ვინც ამ ხილს ღეჭავს. ამგვარად, ძმარი ავითარებს სასიამოვნო ღვინის გემოს, ლიმონის წვენი იქცევა ტკბილ სასმელად და ეფექტი დიდხანს გრძელდება. თუ ყველა ეს ეგზოტიკური ხილი ოდესმე გაშენდება პლანტაციებზე, შაქრის ინდუსტრიას გაცილებით ნაკლები პრობლემა ექნება პროდუქციის ტრანსპორტირებასთან დაკავშირებით. ყოველივე ამის შემდეგ, თაუმატინის პატარა ნაჭერს შეუძლია შეცვალოს გრანულირებული შაქრის მთელი ტომარა! 70-იანი წლების დასაწყისში სინთეზირებული იყო ნაერთი, ყველაზე ტკბილი ყველა სინთეზირებული. ეს არის დიპეპტიდი, რომელიც აგებულია ორი ამინომჟავის - ასპარტისა და ამინომალონის ნარჩენებისგან. დიპეპტიდში ამინომალონური მჟავის ნარჩენების ორი კარბოქსილის ჯგუფი ჩანაცვლებულია მეთანოლითა და ფენქოლით წარმოქმნილი ეთერული ჯგუფებით (ის გვხვდება მცენარეთა ეთერზეთებში და გამოიყოფა ტურპენტინისგან). ეს ნივთიერება დაახლოებით 33000-ჯერ უფრო ტკბილია ვიდრე საქაროზა. იმისათვის, რომ შოკოლადის ფილა ჩვეულებრივად ტკბილი გახდეს, საკმარისია ამ სანელებლის მილიგრამის ფრაქცია.
 რაღაც საინტერესო ცილების შესახებ კანისა და თმის ქიმიური და ფიზიკური თვისებები განისაზღვრება კერატინების თვისებებით. თითოეულ ცხოველურ სახეობაში კერატინს აქვს გარკვეული მახასიათებლები, ამიტომ ეს სიტყვა გამოიყენება მრავლობით რიცხვში. კერატინები ხერხემლიანების წყალში უხსნადი ცილებია, რომლებიც ქმნიან მათ თმას, მატყლს, რქოვანას და ფრჩხილებს. წყლის ზემოქმედებით კანის, თმისა და ფრჩხილების კერატინი რბილდება, შეშუპებულია და წყლის აორთქლების შემდეგ ისევ მკვრივდება. კერატინის მთავარი ქიმიური თვისება ის არის, რომ ის შეიცავს გოგირდის შემცველ ამინომჟავას ცისტეინს 15%-მდე. კერატინის მოლეკულის ცისტეინის ნაწილში არსებული გოგირდის ატომები ადვილად ქმნიან კავშირებს მეზობელი მოლეკულის გოგირდის ატომებთან და წარმოიქმნება დისულფიდური ხიდები, რომლებიც აკავშირებენ ამ მაკრომოლეკულებს. კერატინები არის ფიბრილარული ცილები. ქსოვილებში ისინი არსებობენ გრძელი ძაფების სახით - ფიბრილები, რომლებშიც მოლეკულები განლაგებულია ერთი მიმართულებით მიმართულ ჩალიჩებად. ამ ძაფებში ცალკეული მაკრომოლეკულები ასევე დაკავშირებულია ერთმანეთთან ქიმიური ბმებით (სურ. 1). ხვეული ძაფები ტრიალდება სამმაგი სპირალის სახით და 11 ხვეული გაერთიანებულია მიკროფიბრილად, რომელიც ქმნის თმის ცენტრალურ ნაწილს (იხ. სურ. 2). მიკროფიბრილები გაერთიანებულია მაკროფიბრილების წარმოქმნით. ა) წყალბადი ბ) იონური გ) არაპოლარული დ) დისულფიდური ნახ. 2. თმის კერატინი არის ფიბრილარული ცილა. კავშირები კავშირები ურთიერთქმედების ხიდი ნახ. 1. ჯაჭვის ცილის მოლეკულებს შორის ურთიერთქმედების სახეები
რაღაც საინტერესო ცილების შესახებ კანისა და თმის ქიმიური და ფიზიკური თვისებები განისაზღვრება კერატინების თვისებებით. თითოეულ ცხოველურ სახეობაში კერატინს აქვს გარკვეული მახასიათებლები, ამიტომ ეს სიტყვა გამოიყენება მრავლობით რიცხვში. კერატინები ხერხემლიანების წყალში უხსნადი ცილებია, რომლებიც ქმნიან მათ თმას, მატყლს, რქოვანას და ფრჩხილებს. წყლის ზემოქმედებით კანის, თმისა და ფრჩხილების კერატინი რბილდება, შეშუპებულია და წყლის აორთქლების შემდეგ ისევ მკვრივდება. კერატინის მთავარი ქიმიური თვისება ის არის, რომ ის შეიცავს გოგირდის შემცველ ამინომჟავას ცისტეინს 15%-მდე. კერატინის მოლეკულის ცისტეინის ნაწილში არსებული გოგირდის ატომები ადვილად ქმნიან კავშირებს მეზობელი მოლეკულის გოგირდის ატომებთან და წარმოიქმნება დისულფიდური ხიდები, რომლებიც აკავშირებენ ამ მაკრომოლეკულებს. კერატინები არის ფიბრილარული ცილები. ქსოვილებში ისინი არსებობენ გრძელი ძაფების სახით - ფიბრილები, რომლებშიც მოლეკულები განლაგებულია ერთი მიმართულებით მიმართულ ჩალიჩებად. ამ ძაფებში ცალკეული მაკრომოლეკულები ასევე დაკავშირებულია ერთმანეთთან ქიმიური ბმებით (სურ. 1). ხვეული ძაფები ტრიალდება სამმაგი სპირალის სახით და 11 ხვეული გაერთიანებულია მიკროფიბრილად, რომელიც ქმნის თმის ცენტრალურ ნაწილს (იხ. სურ. 2). მიკროფიბრილები გაერთიანებულია მაკროფიბრილების წარმოქმნით. ა) წყალბადი ბ) იონური გ) არაპოლარული დ) დისულფიდური ნახ. 2. თმის კერატინი არის ფიბრილარული ცილა. კავშირები კავშირები ურთიერთქმედების ხიდი ნახ. 1. ჯაჭვის ცილის მოლეკულებს შორის ურთიერთქმედების სახეები
 რაღაც საინტერესო ცილების შესახებ თმას აქვს ჰეტეროგენული სტრუქტურა ჯვარედინი განყოფილებაში. ქიმიური თვალსაზრისით, თმის ყველა ფენა იდენტურია და შედგება ერთი ქიმიური ნაერთისგან - კერატინი. მაგრამ კერატინის აგებულების ხარისხისა და სახეობიდან გამომდინარე, არსებობს სხვადასხვა თვისებების მქონე ფენები: კუტიკულა - ზედაპირული ქერცლიანი შრე; ბოჭკოვანი, ან კორტიკალური ფენა; ბირთვი. კუტიკულა წარმოიქმნება ბრტყელი უჯრედებისგან, რომლებიც ერთმანეთს თევზის ქერცლებს ჰგავს. კოსმეტიკური თვალსაზრისით, ეს არის თმის ყველაზე მნიშვნელოვანი ფენა. თმის გარეგნობა დამოკიდებულია მის მდგომარეობაზე: ბზინვარება, ელასტიურობა ან, პირიქით, დაბნელება, ბოლოების გაყოფა. კუტიკულის მდგომარეობა ასევე მოქმედებს თმის შეღებვისა და დახვევის პროცესებზე, ვინაიდან იმისათვის, რომ წამლებმა შეაღწიონ თმის ღრმა ფენებში, პიგმენტამდე, აუცილებელია კუტიკულის დარბილება. კერატინი, რომლისგანაც "სასწორი" მზადდება, შეშუპებულია ტენიანობის ზემოქმედებისას, განსაკუთრებით თუ ამას თან ახლავს სითბო და ტუტე პრეპარატები (საპონი). ქიმიური თვალსაზრისით, ეს აიხსნება კერატინის მოლეკულებში წყალბადის ბმების რღვევით, რომლებიც აღდგება თმის გაშრობისას. როდესაც ფირფიტები იშლება, მათი კიდეები ვერტიკალურად დგება და თმა კარგავს ბზინვარებას. კუტიკულის დარბილება ასევე ამცირებს თმის მექანიკურ სიმტკიცეს: სველის დროს უფრო ადვილია მისი დაზიანება. სასწორის კიდეებს შორის სივრცე ივსება ცხიმიანი ცხიმით, რომელიც ანიჭებს თმას ბზინვარებას, რბილობას და ელასტიურობას. ბოჭკოვანი, ანუ კორტიკალური ფენა წარმოიქმნება ერთი მიმართულებით განლაგებული გრძელი შუბლის ფორმის კერატინიზებული უჯრედებით; მასზეა დამოკიდებული თმის ელასტიურობა და ელასტიურობა. ეს ფენა შეიცავს პიგმენტ მელანინს, რომელიც "პასუხისმგებელია" თმის ფერზე. თმის ფერი დამოკიდებულია მასში მელანინისა და ჰაერის ბუშტების არსებობაზე. ქერა თმა შეიცავს გაფანტულ პიგმენტს, მუქი თმა შეიცავს მარცვლოვან პიგმენტს. ბირთვი, ანუ მედულა, შედგება არასრულად კერატინიზებული უჯრედებისგან.
რაღაც საინტერესო ცილების შესახებ თმას აქვს ჰეტეროგენული სტრუქტურა ჯვარედინი განყოფილებაში. ქიმიური თვალსაზრისით, თმის ყველა ფენა იდენტურია და შედგება ერთი ქიმიური ნაერთისგან - კერატინი. მაგრამ კერატინის აგებულების ხარისხისა და სახეობიდან გამომდინარე, არსებობს სხვადასხვა თვისებების მქონე ფენები: კუტიკულა - ზედაპირული ქერცლიანი შრე; ბოჭკოვანი, ან კორტიკალური ფენა; ბირთვი. კუტიკულა წარმოიქმნება ბრტყელი უჯრედებისგან, რომლებიც ერთმანეთს თევზის ქერცლებს ჰგავს. კოსმეტიკური თვალსაზრისით, ეს არის თმის ყველაზე მნიშვნელოვანი ფენა. თმის გარეგნობა დამოკიდებულია მის მდგომარეობაზე: ბზინვარება, ელასტიურობა ან, პირიქით, დაბნელება, ბოლოების გაყოფა. კუტიკულის მდგომარეობა ასევე მოქმედებს თმის შეღებვისა და დახვევის პროცესებზე, ვინაიდან იმისათვის, რომ წამლებმა შეაღწიონ თმის ღრმა ფენებში, პიგმენტამდე, აუცილებელია კუტიკულის დარბილება. კერატინი, რომლისგანაც "სასწორი" მზადდება, შეშუპებულია ტენიანობის ზემოქმედებისას, განსაკუთრებით თუ ამას თან ახლავს სითბო და ტუტე პრეპარატები (საპონი). ქიმიური თვალსაზრისით, ეს აიხსნება კერატინის მოლეკულებში წყალბადის ბმების რღვევით, რომლებიც აღდგება თმის გაშრობისას. როდესაც ფირფიტები იშლება, მათი კიდეები ვერტიკალურად დგება და თმა კარგავს ბზინვარებას. კუტიკულის დარბილება ასევე ამცირებს თმის მექანიკურ სიმტკიცეს: სველის დროს უფრო ადვილია მისი დაზიანება. სასწორის კიდეებს შორის სივრცე ივსება ცხიმიანი ცხიმით, რომელიც ანიჭებს თმას ბზინვარებას, რბილობას და ელასტიურობას. ბოჭკოვანი, ანუ კორტიკალური ფენა წარმოიქმნება ერთი მიმართულებით განლაგებული გრძელი შუბლის ფორმის კერატინიზებული უჯრედებით; მასზეა დამოკიდებული თმის ელასტიურობა და ელასტიურობა. ეს ფენა შეიცავს პიგმენტ მელანინს, რომელიც "პასუხისმგებელია" თმის ფერზე. თმის ფერი დამოკიდებულია მასში მელანინისა და ჰაერის ბუშტების არსებობაზე. ქერა თმა შეიცავს გაფანტულ პიგმენტს, მუქი თმა შეიცავს მარცვლოვან პიგმენტს. ბირთვი, ანუ მედულა, შედგება არასრულად კერატინიზებული უჯრედებისგან.
ცოცხალი ორგანიზმი, რომელსაც აქვს უნიკალური სტრუქტურული ორგანიზაცია, რომელიც უზრუნველყოფს მის ფენოტიპურ მახასიათებლებსა და ბიოლოგიურ ფუნქციებს, თავის სტრუქტურულ და ფუნქციურ ერთიანობაში ეყრდნობა ცილოვან სხეულებს (ცილებს). ეს ფილოსოფიური და თეორიული იდეა, რომელიც ეფუძნება მისი პერიოდის ბუნებისმეტყველების შედარებით მცირე მიღწევებს, წამოაყენა ფ. ენგელსმა, რომელიც თავის ნაშრომებში აღნიშნავს, რომ „ყოველგან, სადაც ცხოვრებას ვხვდებით, ვხვდებით, რომ ის ასოცირდება ცილოვან სხეულთან. და ყველგან, სადაც ვხვდებით რომელიმე ცილოვან სხეულს, რომელიც არ არის დაშლის პროცესში, ჩვენ, გამონაკლისის გარეშე, ვხვდებით სიცოცხლის ფენომენებს“ (ციტ. Engels F. Anti-dühring. 1950, გვ. 77).
ცილოვანი ნივთიერებების შესახებ იდეების განვითარება
ცილების, როგორც ნაერთების კლასის იდეა ჩამოყალიბდა მე-18-მე-19 საუკუნეებში. ამ პერიოდის განმავლობაში, მსგავსი თვისებების მქონე ნივთიერებები იზოლირებული იყო ცოცხალი სამყაროს სხვადასხვა ობიექტებიდან (თესლები და მცენარეების წვენი, კუნთები, თვალის ლინზა, სისხლი, რძე და ა. გაშრობისას რქისმაგვარი მასა მიიღება „ცეცხლით ანალიზის დროს“, იგრძნობოდა დამწვარი მატყლის ან რქის სუნი და გამოდიოდა ამიაკი. ბეკარიმ, რომელმაც 1728 წელს ხორბლის ფქვილისგან პირველი ცილოვანი ნივთიერება გამოყო, მას "წებოვანა" უწოდა. მან ასევე აჩვენა თავისი მსგავსება ცხოველური წარმოშობის პროდუქტებთან და ვინაიდან ყველა ეს მსგავსი თვისება ცნობილი იყო კვერცხის ცილისთვის, ნივთიერებების ახალ კლასს ცილები ეწოდა.
ცილების სტრუქტურის შესწავლაში მნიშვნელოვანი როლი ითამაშა მჟავებითა და საჭმლის მომნელებელი წვენებით მათი დაშლის მეთოდების შემუშავებამ. 1820 წელს ა. ბრაკონო (საფრანგეთი) ცხოველების კანს და სხვა ქსოვილებს გოგირდმჟავას მრავალი საათის განმავლობაში უტარებდა, შემდეგ გაანეიტრალა ნარევი და მიიღო ფილტრატი, რომლის აორთქლებისას ნივთიერების კრისტალები მას გლიკოკოლს უწოდებდა ("წებოვანი შაქარი"). ნალექი. ეს იყო ცილებისგან გამოყოფილი პირველი ამინომჟავა. მისი სტრუქტურული ფორმულა შეიქმნა 1846 წელს.
1838 წელს, სხვადასხვა ცილების ელემენტარული შემადგენლობის სისტემატური შესწავლის შემდეგ, რომელშიც აღმოჩენილია ნახშირბადი, წყალბადი, აზოტი, ჟანგბადი, გოგირდი და ფოსფორი, ჰოლანდიელმა ქიმიკოსმა და ექიმმა G. J. Mulder-მა (1802-1880) შემოგვთავაზა სტრუქტურის პირველი თეორია. ცილების - თეორია ცილის. ელემენტარული შემადგენლობის კვლევების საფუძველზე, მალდერი მივიდა დასკვნამდე, რომ ყველა ცილა შეიცავს ერთ ან მეტ ჯგუფს ("რადიკალებს") C 40 H 62 N 10 O 2 გოგირდთან ან ფოსფორთან ან ორივესთან ერთად. მან შემოგვთავაზა ტერმინი "ცილა" ამ ჯგუფის აღსანიშნავად (ბერძნული პროტოსიდან - პირველი, ყველაზე მნიშვნელოვანი), რადგან მას სჯეროდა, რომ ეს ნივთიერება "უდავოდ არის ყველაზე მნიშვნელოვანი ორგანული სამეფოს ყველა ცნობილი ორგანოდან და მის გარეშე. , როგორც ჩანს, ჩვენს პლანეტაზე სიცოცხლე არ შეიძლება იყოს“ (ციტირებულია წიგნიდან: Shamin A.N. History of protein chemistry. M.: Nauka, 1977. გვ. 80.). ასეთი ჯგუფის არსებობის იდეა მალევე უარყვეს და შეიცვალა ტერმინი "ცილები" მნიშვნელობა და ახლა გამოიყენება ტერმინის "ცილების" სინონიმად.
შემდგომმა კვლევამ ეს შესაძლებელი გახადა მე-19 საუკუნის ბოლოს. პროტეინებისგან ათზე მეტი ამინომჟავის იზოლირება. ა.იას მიერ ცილის ჰიდროლიზის პროდუქტების შესწავლის შედეგებზე დაყრდნობით. დანილევსკი იყო პირველი, ვინც ვარაუდობდა -NH-CO- ობლიგაციების არსებობას ცილებში, როგორც ბიურეტში, და 1888 წელს წამოაყენა ჰიპოთეზა ცილის სტრუქტურის შესახებ, სახელწოდებით "ელემენტარული სერიის თეორია", ხოლო გერმანელმა ქიმიკოსმა ე. ფიშერმა, ჰოფმაისტერთან ერთად, მიიღო კრისტალური ცილა - კვერცხის ალბუმინი, შემოთავაზებული 1902 წელს ცილის სტრუქტურის პეპტიდური თეორია.
ე. ფიშერის მუშაობის შედეგად გაირკვა, რომ ცილები არის ამინომჟავების წრფივი პოლიმერები, რომლებიც დაკავშირებულია ერთმანეთთან ამიდური (პეპტიდური) ბმით და ამ კლასის ნაერთების წარმომადგენლების მთელი მრავალფეროვნება შეიძლება აიხსნას განსხვავებებით. ამინომჟავების შემადგენლობაში და პოლიმერულ ჯაჭვში სხვადასხვა ამინომჟავების მონაცვლეობის რიგითობაში. თუმცა, ამ თვალსაზრისმა მაშინვე არ მოიპოვა საყოველთაო აღიარება: კიდევ სამი ათწლეულის განმავლობაში, გაჩნდა ცილის სტრუქტურის სხვა თეორიები, განსაკუთრებით ის, რაც დაფუძნებულია იმ აზრზე, რომ ამინომჟავები არ არიან ცილების სტრუქტურული ელემენტები, არამედ წარმოიქმნება როგორც მეორადი. პროდუქტები ცილების დაშლის დროს მჟავების ან ტუტეების თანდასწრებით.
შემდგომი კვლევა მიზნად ისახავდა ცილების მოლეკულური წონის განსაზღვრას 1925-1930 წლებში შექმნილი ულტრაცენტრიფუგის გამოყენებით. სანჯერი და ცილების მიღება კრისტალური სახით, რაც წამლის სიწმინდის (ერთგვაროვნების) სანდო მტკიცებულებაა. კერძოდ, 1926 წელს დ.სამნერმა თხრილის თესლიდან გამოყო ცილა (ფერმენტი) ურეაზა კრისტალურ მდგომარეობაში; დ.ნორტროპი და მ.კუნიცი 1930-1931 წლებში. მიღებული პეპსინისა და ტრიპსინის კრისტალები.
1951 წელს პაულინგმა და კორიმ შეიმუშავეს ცილის მეორადი სტრუქტურის მოდელი, რომელსაც ალფა სპირალი ეწოდება. 1952 წელს ლინდერსტრომ-ლანგმა შესთავაზა ცილის მოლეკულის ორგანიზების სამი დონის არსებობა: პირველადი, მეორადი, მესამეული. 1953 წელს სანჯერმა პირველად გაშიფრა ამინომჟავების თანმიმდევრობა ინსულინში. 1956 წელს მურმა და სტეინმა შექმნეს პირველი ავტომატური ამინომჟავების ანალიზატორი. 1958 წელს კენდრიუმ და 1959 წელს პერუცმა გაშიფრეს ცილების სამგანზომილებიანი სტრუქტურები - მიოგლობინი და ჰემოგლობინი. 1963 წელს ცანგმა მოახდინა ბუნებრივი ცილოვანი ინსულინის სინთეზირება.
ამგვარად, ცნობილი პოზიცია სიცოცხლის ბუნების შესახებ: „სიცოცხლე არის ცილოვანი სხეულების არსებობის გზა“, რომელიც ჩამოყალიბდა ფ. ენგელსის მიერ, თანდათან მიიღო სანდო სამეცნიერო დადასტურება.
| ცხრილი 1. ცილის შემცველობა ადამიანის ორგანოებსა და ქსოვილებში | |||||
| ორგანოები და ქსოვილები | ცილის შემცველობა, % | ორგანოები და ქსოვილები | ცილის შემცველობა, % | ||
| მშრალი ქსოვილის წონის მიხედვით | სხეულის მთლიანი ცილისგან | მშრალი ქსოვილის წონის მიხედვით | სხეულის მთლიანი ცილისგან | ||
| ტყავი | 63 | 11,5 | ელენთა | 84 | 0,2 |
| ძვლები (მყარი ქსოვილი) | 20 | 18,7 | თირკმლები | 72 | 0,5 |
| კბილები (მყარი ქსოვილები) | 18 | 0,1 | პანკრეასი | 47 | 0,1 |
| განივზოლიანი კუნთები | 80 | 34,7 | Საჭმლის მომნელებელი სისტემა | 63 | 1,8 |
| ტვინის და ნერვული ქსოვილი | 45 | 2,0 | ცხიმოვანი ქსოვილი | 14 | 6,4 |
| ღვიძლი | 57 | 3,6 | სხვა თხევადი ქსოვილები: | 85 | 1,4 |
| გული | 60 | 0,7 | სხვა მკვრივი ქსოვილები | 54 | 14,6 |
| ფილტვები | 82 | 3,7 | Მთელი სხეული | 45 | 100 |
ახლა აბსოლუტურად საიმედოდ დადგინდა, რომ ცილები (ცილოვანი ნივთიერებები) წარმოადგენს ყველა ცოცხალი ორგანიზმის საფუძველს, სტრუქტურას და ფუნქციებს, რომლებიც ხასიათდება ცილის სტრუქტურების მრავალფეროვნებით და მათი მაღალი მოწესრიგებით; ეს უკანასკნელი არსებობს დროსა და სივრცეში. ცოცხალი ორგანიზმების გასაოცარი უნარი გამრავლების საკუთარი სახის ასევე დაკავშირებულია ცილებს. შეკუმშვა და მოძრაობა - ცოცხალი სისტემების შეუცვლელი ატრიბუტები - პირდაპირ კავშირშია კუნთოვანი აპარატის ცილოვან სტრუქტურებთან. დაბოლოს, სიცოცხლე წარმოუდგენელია მეტაბოლიზმის, ცოცხალი ორგანიზმის შემადგენელი ნაწილების მუდმივი განახლების გარეშე, ანუ ანაბოლიზმისა და კატაბოლიზმის პროცესების გარეშე (ცოცხალი არსებების დაპირისპირების ეს საოცარი ერთობა), რომლებიც დაფუძნებულია კატალიზურად აქტიური ცილების აქტივობაზე. - ფერმენტები.
მოლეკულური ბიოლოგიის ერთ-ერთი დამაარსებლის, ფ. კრიკის ფიგურალური გამოხატვის მიხედვით, ცილები მნიშვნელოვანია, პირველ რიგში, იმიტომ, რომ მათ შეუძლიათ შეასრულონ მრავალფეროვანი ფუნქციები და არაჩვეულებრივი სიმარტივით და მადლით. დადგენილია, რომ ბუნებაში გვხვდება დაახლოებით 10 10-10 12 სხვადასხვა ცილა, რაც უზრუნველყოფს ორგანიზაციის სხვადასხვა სირთულის 10 6 სახეობის ცოცხალი ორგანიზმის არსებობას, დაწყებული ვირუსებიდან ადამიანებამდე. ბუნებრივი ცილების ამ უზარმაზარი რაოდენობით ცნობილია უმნიშვნელო ნაწილის ზუსტი სტრუქტურა და სტრუქტურა - არაუმეტეს 2500. თითოეულ ორგანიზმს ახასიათებს ცილების უნიკალური ნაკრები. ფენოტიპური მახასიათებლები და ფუნქციების მრავალფეროვნება განპირობებულია ამ ცილების ასოციაციის სპეციფიკით, ხშირ შემთხვევაში სუპრამოლეკულური და მულტიმოლეკულური სტრუქტურების სახით, რაც თავის მხრივ განსაზღვრავს უჯრედების და მათი ორგანელების ულტრასტრუქტურას.
E. coli უჯრედი შეიცავს დაახლოებით 3000 სხვადასხვა ცილას, ხოლო ადამიანის ორგანიზმი შეიცავს 50000-ზე მეტ სხვადასხვა ცილას. ყველაზე გასაოცარი ის არის, რომ ყველა ბუნებრივი ცილა შედგება დიდი რაოდენობით შედარებით მარტივი სტრუქტურული ბლოკებისგან, რომლებიც წარმოდგენილია მონომერული მოლეკულებით - ამინომჟავებით, რომლებიც დაკავშირებულია ერთმანეთთან პოლიპეპტიდურ ჯაჭვებში. ბუნებრივი ცილები აგებულია 20 სხვადასხვა ამინომჟავისგან. ვინაიდან ეს ამინომჟავები შეიძლება გაერთიანდეს ძალიან განსხვავებული თანმიმდევრობით, მათ შეუძლიათ შექმნან ცილების უზარმაზარი მრავალფეროვნება. იზომერების რაოდენობა, რომელთა მიღებაც შესაძლებელია პოლიპეპტიდში ამინომჟავების მითითებული რაოდენობის ყველა შესაძლო პერმუტაციით, უზარმაზარია. ასე რომ, თუ ორი ამინომჟავისგან შესაძლებელია მხოლოდ ორი იზომერის წარმოქმნა, მაშინ ოთხი ამინომჟავიდან თეორიულად შესაძლებელია 24 იზომერის წარმოქმნა, ხოლო 20 ამინომჟავისგან - 2,4 x 10 18 სხვადასხვა ცილა.
ძნელი არ არის იმის პროგნოზირება, რომ ცილის მოლეკულაში განმეორებადი ამინომჟავების ნარჩენების რაოდენობის მატებასთან ერთად, შესაძლო იზომერების რაოდენობა იზრდება ასტრონომიულ მნიშვნელობებამდე. ნათელია, რომ ბუნება არ დაუშვებს ამინომჟავების თანმიმდევრობების შემთხვევით კომბინაციებს და თითოეულ სახეობას ახასიათებს ცილების საკუთარი სპეციფიკური ნაკრები, რომელიც განისაზღვრება, როგორც ახლა ცნობილია, ცოცხალი ორგანიზმების დნმ-ის მოლეკულაში კოდირებული მემკვიდრეობითი ინფორმაციით. ეს არის ინფორმაცია, რომელიც შეიცავს დნმ-ის ნუკლეოტიდების ხაზოვან თანმიმდევრობას, რომელიც განსაზღვრავს ამინომჟავების ხაზოვან თანმიმდევრობას სინთეზირებული ცილის პოლიპეპტიდურ ჯაჭვში. შედეგად მიღებული ხაზოვანი პოლიპეპტიდური ჯაჭვი ახლა დაჯილდოებულია ფუნქციური ინფორმაციით, რომლის მიხედვითაც იგი სპონტანურად გარდაიქმნება გარკვეულ სტაბილურ სამგანზომილებიან სტრუქტურაში. ამრიგად, ლაბილური პოლიპეპტიდური ჯაჭვი იკეცება და ტრიალებს ცილის მოლეკულის სივრცულ სტრუქტურაში, არა შემთხვევით, არამედ ამინომჟავების თანმიმდევრობაში მოცემული ინფორმაციის მკაცრი დაცვით.
ადამიანებისა და ცხოველების ქსოვილები და ორგანოები ყველაზე მდიდარია ცილოვანი ნივთიერებებით. ამ ცილების უმეტესობა წყალში ძალიან ხსნადია. ამასთან, ხრტილის, თმის, ფრჩხილების, რქების, ძვლის ქსოვილისგან იზოლირებული ზოგიერთი ორგანული ნივთიერება - წყალში უხსნადი - ასევე კლასიფიცირდება როგორც ცილები, რადგან მათი ქიმიური შემადგენლობა ახლოს იყო კუნთოვანი ქსოვილის, სისხლის შრატისა და კვერცხების ცილებთან. ცილების რაოდენობრივი შემცველობა ადამიანის სხვადასხვა ქსოვილებსა და ორგანოებში მოცემულია ცხრილში. 1.1. კუნთებში, ფილტვებში, ელენთაში, თირკმელებში, ცილები შეადგენს მშრალი მასის 70-80%-ზე მეტს, ხოლო მთლიანი ადამიანის ორგანიზმში მშრალი მასის 45-50%-მდე.
მიკროორგანიზმები და მცენარეები ასევე ცილის წყაროა. ცხოველური ქსოვილებისგან განსხვავებით, მცენარეები შეიცავს მნიშვნელოვნად ნაკლებ ცილებს (ცხრილი 2).
ცილების განაწილება უჯრედქვეშა სტრუქტურებს შორის არათანაბარია: მათი უმეტესობა უჯრედის წვენშია (ჰიალოპლაზმა) (ცხრილი 3). ცილების შემცველობა ორგანელებში უფრო მეტად განისაზღვრება უჯრედში არსებული ორგანელების ზომითა და რაოდენობით.
ცილების ქიმიური შემადგენლობის, სტრუქტურისა და თვისებების შესასწავლად, ისინი ჩვეულებრივ იზოლირებულია თხევადი ქსოვილებიდან ან ცილებით მდიდარი ცხოველური ორგანოებიდან, მაგალითად, სისხლის შრატი, რძე, კუნთები, ღვიძლი, კანი, თმა, მატყლი.
ცილა და მისი დამახასიათებელი თვისებები
ცილების ელემენტარული შემადგენლობა (ცხრილი 4.) მშრალი ნივთიერებით წარმოდგენილია 50-54% ნახშირბადით, 21-23% ჟანგბადით, 6.5-7.3% წყალბადით, 15-17% აზოტით, 0.3-2.5 გოგირდით და 0.5-მდე. % ნაცარი. ზოგიერთი ცილა ასევე შეიცავს მცირე რაოდენობით ფოსფორს, რკინას, მანგანუმს, მაგნიუმს, იოდს და ა.შ.
ამრიგად, ნახშირბადის, ჟანგბადისა და წყალბადის გარდა, რომლებიც თითქმის ყველა ორგანული პოლიმერული მოლეკულის ნაწილია, აზოტი ცილების აუცილებელი კომპონენტია და ამიტომ ცილებს ჩვეულებრივ მოიხსენიებენ, როგორც აზოტის შემცველ ორგანულ ნივთიერებებს. აზოტის შემცველობა მეტ-ნაკლებად მუდმივია ყველა ცილაში (საშუალოდ 16%), ამიტომ ზოგჯერ ბიოლოგიურ ობიექტებში ცილის რაოდენობა განისაზღვრება ცილის აზოტის რაოდენობით: ანალიზის დროს ნაპოვნი აზოტის მასა მრავლდება კოეფიციენტზე. 6.25 (100: 16 = 6.25). მაგრამ ზოგიერთი ცილისთვის ეს თვისება ატიპიურია. მაგალითად, პროტამინებში აზოტის შემცველობა აღწევს 30%-ს, შესაბამისად, მხოლოდ ელემენტარული შემადგენლობით შეუძლებელია ცილის ზუსტად გარჩევა ორგანიზმში არსებული სხვა აზოტის შემცველი ნივთიერებებისგან.
ამრიგად, ელემენტარული შემადგენლობის გათვალისწინებით, ცილები არის მაღალმოლეკულური აზოტის შემცველი ორგანული ნივთიერებები, რომლებიც შედგება ამინომჟავებისგან, რომლებიც დაკავშირებულია ჯაჭვებში პეპტიდური ბმების გამოყენებით და აქვთ რთული სტრუქტურული ორგანიზაცია. ეს განმარტება აერთიანებს ცილების დამახასიათებელ მახასიათებლებს, რომელთა შორისაა შემდეგი:
- აზოტის საკმაოდ მუდმივი წილი (საშუალოდ მშრალი წონის 16%);
- მუდმივი სტრუქტურული ერთეულების - ამინომჟავების არსებობა;
- პეპტიდური ბმები ამინომჟავებს შორის, რომელთა დახმარებით ისინი დაკავშირებულია პოლიპეპტიდურ ჯაჭვებში;
- დიდი მოლეკულური წონა (4-5 ათასიდან რამდენიმე მილიონ დალტონამდე);
- პოლიპეპტიდური ჯაჭვის რთული სტრუქტურული ორგანიზაცია, რომელიც განსაზღვრავს ცილების ფიზიკურ-ქიმიურ და ბიოლოგიურ თვისებებს.
ცილების სტრუქტურული ერთეულები, ანუ მონომერები შეიძლება გამოვლინდეს ჰიდროლიზის შემდეგ: მჟავე (HCl), ტუტე (Ba(OH) 2) და/ან ნაკლებად ხშირად ფერმენტული. ეს ტექნიკა ყველაზე ხშირად გამოიყენება ცილების შემადგენლობის შესასწავლად. დადგენილია, რომ სუფთა ცილის ჰიდროლიზისას, რომელიც არ შეიცავს მინარევებს, გამოიყოფა 20-მდე სხვადასხვა L-სერიის α-ამინომჟავები, რომლებიც წარმოადგენენ ცილის მონომერებს. პროტეინებში ამინომჟავები ჯაჭვში არის დაკავშირებული კოვალენტური პეპტიდური ბმებით.
α-ამინომჟავები არის კარბოქსილის მჟავების წარმოებულები, რომლებშიც წყალბადის ერთი ატომი, α-ნახშირბადი, ჩანაცვლებულია ამინოჯგუფით (-NH 2), მაგალითად:
ცილების მოლეკულური წონა . ცილების ყველაზე მნიშვნელოვანი მახასიათებელი მათი მაღალი მოლეკულური წონაა. ჯაჭვის სიგრძიდან გამომდინარე, ყველა პოლიპეპტიდი შეიძლება დაიყოს პეპტიდებად (შეიცავს 2-დან 10 ამინომჟავამდე), პოლიპეპტიდებად (10-დან 40 ამინომჟავამდე) და ცილებად (40-ზე მეტი ამინომჟავა). თუ ერთი ამინომჟავის საშუალო მოლეკულურ წონას მივიღებთ დაახლოებით 100, მაშინ პეპტიდების მოლეკულური წონა უახლოვდება 1000-ს, პოლიპეპტიდებს - 4000-მდე, ხოლო ცილებს - 4-5 ათასიდან რამდენიმე მილიონამდე (ცხრილი 5.)
ცილების რთული სტრუქტურული ორგანიზაცია . ზოგიერთ ბუნებრივ პოლიპეპტიდს (ჩვეულებრივ, ერთი ამინომჟავისგან შედგება) და ხელოვნურად მიღებულ პოლიპეპტიდს აქვს დიდი მოლეკულური წონა, მაგრამ ისინი არ შეიძლება კლასიფიცირდეს ცილებად. უნიკალური თვისება, რაც მათ ცილებისგან განასხვავებს, არის ცილების დენატურაციის უნარი, ანუ დამახასიათებელი ფიზიკურ-ქიმიური თვისებების დაკარგვა და, რაც მთავარია, ბიოლოგიური ფუნქციები, ნივთიერებების მოქმედებით, რომლებიც არ არღვევენ პეპტიდურ კავშირებს. დენატურაციის უნარი მიუთითებს ცილის მოლეკულის კომპლექსურ სივრცულ ორგანიზაციაზე, რომელიც არ არსებობს ჩვეულებრივ პოლიპეპტიდებში.
| Გვერდი 1 | სულ გვერდები: 7 |
ახალი მიმოხილვის თანახმად, რომელიც გამოქვეყნდა ვებგვერდზე Applied Physiology, Nutrition and Metabolism, მნიშვნელოვანია არა მხოლოდ თქვენ მიერ მოხმარებული ცილის რაოდენობა, არამედ მისი წყაროც. ამაზე ზრუნვის სამი მიზეზი არსებობს.
უპირველეს ყოვლისა, ცილის ნებისმიერი წყარო, იქნება ეს ქათამი თუ არაქისი, შეიცავს სხვადასხვა რაოდენობით ამინომჟავებს - ცილების სამშენებლო ბლოკებს. 20 შესაძლო ამინომჟავიდან ცხრა უბრალოდ აუცილებელია ორგანიზმისთვის. ამ ამინომჟავების მიღება შეგიძლიათ მხოლოდ საკვებიდან. ამიტომ ძალიან მნიშვნელოვანია ცილებით მდიდარი სხვადასხვა საკვების სწორად შეყვანა.
ცხოველური წარმოშობის პროდუქტები (ხორცი, კვერცხი, რძის პროდუქტები) შეიცავს ყველა აუცილებელ ამინომჟავას სხვადასხვა რაოდენობით, მაგრამ მცენარეული პროდუქტების უმეტესობა შეიცავს ცხრა აუცილებელი ამინომჟავის მხოლოდ ფრაქციებს.
„ეს ნიშნავს, რომ თუ თქვენ აირჩევთ პროტეინის მიღებას მხოლოდ თხილისგან, თქვენი სხეული მოკლებული იქნება მნიშვნელოვანი ამინომჟავებისგან“, - განმარტავს კვლევის თანაავტორი რაჯაველ ელანგო, კვების და მეტაბოლიზმის სპეციალისტი.
როდესაც თქვენ იღებთ ცილებს მცენარეული საკვებიდან, მნიშვნელოვანია აირჩიოთ სწორი ტიპები და რაოდენობა, რათა უზრუნველყოთ თქვენი ყოველდღიური საჭიროების სრული მიღება აუცილებელი ამინომჟავების შესახებ.
რა თქმა უნდა, ეს არ არის იმის მიზეზი, რომ უარი თქვათ კვების პრეფერენციებზე და მიიღოთ მხოლოდ ცილები, მიირთვათ ისინი საუზმეზე, ლანჩზე და სადილზე. ასეთი დიეტა, გარდა ცილისა, შეიცავს დიდი რაოდენობით კალორიებს, ცხიმებსა და ქოლესტერინს, რაც უარყოფითად აისახება თქვენს ფიგურაზე და მთლიან ჯანმრთელობაზე. და ეს არის მეორე მიზეზი, რომ უყუროთ რა საკვებს ირჩევთ თქვენი ორგანიზმის ცილებით გაჯერებისთვის.
და ბოლოს, მესამე მიზეზი ყველაზე მნიშვნელოვანია. „ყოველი საკვები, რომელიც გაწვდით პროტეინს, შეიცავს ვიტამინებისა და მინერალების გარკვეულ რაოდენობას“, - ამბობს ილანგო. „ზოგიერთი საკვები მდიდარია B ვიტამინით, ზოგი მდიდარია რკინით, ზოგი კი პრაქტიკულად არ შეიცავს საკვებ ნივთიერებებს“.
თქვენი ორგანიზმი ვერ შეძლებს მიღებულ პროტეინს მაქსიმალურ სარგებელს აითვისოს, თუ მნიშვნელოვანი საკვები ნივთიერებების ნაკლებობაა.
გსურთ დარწმუნდეთ, რომ იღებთ თქვენს პროტეინს სწორი საკვებიდან? აქ არის ცილის რამდენიმე ყველაზე ჯანსაღი წყარო.
კვერცხები
liz west/Flickr.com„თითოეული კვერცხი არა მხოლოდ შეიცავს 6 გრამ პროტეინს, არამედ ის ასევე არის ყველაზე ჯანსაღი ცილა“, - ამბობს ბონი ტოუბ-დიქსი, ამერიკელი დიეტოლოგი, ბლოგერი და წიგნის „Read Before You Eat“-ის ავტორი.
კვერცხებიდან მიღებულ პროტეინს აქვს ყველაზე მაღალი მონელება და ხელს უწყობს სხეულის ქსოვილების ფორმირებას. გარდა ამისა, კვერცხები მდიდარია ქოლინით და ვიტამინებით B 12 და D - ნივთიერებები, რომლებიც მნიშვნელოვანია ენერგიის საერთო დონის შესანარჩუნებლად და ორგანიზმის უჯრედებში მისი მიწოდებისთვის.
მიუხედავად გავრცელებული მოსაზრებისა, რომ კვერცხებიდან ქოლესტერინი უარყოფითად მოქმედებს გულის მუშაობაზე, რის შედეგადაც ამ პროდუქტის მიღება შეიძლება კვირაში არაუმეტეს 2-3-ჯერ, მეცნიერებმა საპირისპირო დაადასტურეს. British Medical Journal-ში გამოქვეყნებულმა კვლევამ აჩვენა, რომ დღეში ერთი კვერცხი არ მოქმედებს გულის მუშაობაზე და არ ზრდის ინსულტის რისკს.
Ხაჭო
„150 გრ ხაჭოს ერთი პორცია შეიცავს დაახლოებით 25 გრ პროტეინს და კალციუმის ყოველდღიური ღირებულების 18%-ს“, ამბობს დიეტოლოგი ჯიმ უაითი. გარდა ამისა, ხაჭო მდიდარია კაზინით, ნელა ასათვისებელი ცილა, რომელიც ბლოკავს შიმშილის გრძნობას რამდენიმე საათის განმავლობაში.
ქათამი
 ჯეიმს / Flickr.com
ჯეიმს / Flickr.com ფრინველი უნდა იყოს ცილოვანი დიეტის საფუძველი. ის შეიცავს ნაკლებ გაჯერებულ ცხიმებს, ვიდრე სხვა ხორცს და დაახლოებით 40 გრ პროტეინს თითო მკერდზე (20 გრ ცილა 100 გრ ხორცზე). ილანგო გვირჩევს, რაც შეიძლება ხშირად აირჩიოთ თეთრი ხორცი, რომ ნაკლები კალორია მოიხმაროთ.
მთელი მარცვლეული
მთლიანი მარცვლეული პროდუქტები ჯანსაღია და შეიცავს ბევრად მეტ ცილას, ვიდრე ჩვეულებრივი ფქვილის პროდუქტები. მაგალითად, პირველი კლასის ხორბლის ფქვილისგან დამზადებული პური შეიცავს 7 გ ცილას, ხოლო მთლიანი მარცვლეულის პური შეიცავს 9 გ ცილას 100 გრ პროდუქტზე.
რაც მთავარია, მარცვლეული შეიცავს ბოჭკოებს, კარგია გულისთვის და ხელს უწყობს წონის კონტროლს.
თევზი
 ჯეიმს ბოუ / Flickr.com
ჯეიმს ბოუ / Flickr.com „დაბალკალორიული და საკვები ნივთიერებებით დატვირთული თევზი ომეგა -3 ცხიმოვანი მჟავების შესანიშნავი წყაროა, რომელიც ხელს უწყობს გულის ჯანმრთელობას და ასტაბილურებს განწყობას“, - ამბობს ტაუბ-დიქსი.
ყველაზე ჯანსაღ თევზებს შორისაა ორაგული და ტუნა. ორაგულის ერთი პორცია შეიცავს დაახლოებით 20 გ ცილას და 6,5 გ უჯერი ცხიმოვან მჟავებს. ტუნა კი ცილის ნამდვილი საწყობია: 25 გრ 100 გრ პროდუქტზე.
თუ სხეულის ჭარბი ცხიმისგან თავის დაღწევა გსურთ, დიეტაში ორაგულიც უნდა შეიტანოთ: შეიცავს მხოლოდ 10-12 გ ცხიმს, გაჯერებულ და უჯერი. დიეტოლოგები გვირჩევენ თევზის ჭამას კვირაში ორჯერ, გამომცხვარი ან შემწვარი.
პარკოსნები
 cookbookman17/Flickr.com
cookbookman17/Flickr.com ბერძნული (გაფილტრული) იოგურტი
ბერძნული იოგურტი შეიძლება იყოს საუზმე, საჭმელი ან ინგრედიენტი სხვადასხვა კერძებში. ჩვეულებრივ იოგურტთან შედარებით, ბერძნულ იოგურტს აქვს თითქმის ორჯერ მეტი ცილა: 5-10 გ-ის ნაცვლად იოგურტის ერთ პორციაში, ის არის 13-20 გ. გარდა ამისა, ბერძნულ იოგურტს აქვს საკმაოდ ბევრი კალციუმი: დღიურის 20%. ღირებულება.
თხილი
 ადამ უაილსი/Flickr.com
ადამ უაილსი/Flickr.com თხილი ცნობილია იმით, რომ მდიდარია ჯანსაღი უჯერი ცხიმოვანი მჟავებით, მაგრამ ასევე მდიდარია ცილებით. გარდა ამისა, 2013 წელს გამოქვეყნებულმა კვლევამ, რომელიც გამოქვეყნდა New England Journal of Medicine-ში, აჩვენა, რომ ადამიანები, რომლებიც დღეში მუჭა თხილს მიირთმევდნენ, 20%-ით ნაკლები აქვთ დაავადებისგან სიკვდილის რისკი.
გამწვანება
 ჯეისონ ბაჩმანი/Flickr.com
ჯეისონ ბაჩმანი/Flickr.com სხვადასხვა სახის მწვანილი და მწვანე ფოთლოვანი ბოსტნეული მდიდარია ცილებით. მაგალითად, 100 გრ ისპანახი შეიცავს მხოლოდ 22 კკალს და დაახლოებით 3 გრ პროტეინს, ხოლო ოხრახუში შეიცავს 47 კკალს და 3,7 გრ ცილას. მიუხედავად იმისა, რომ მწვანილი არ შეიცავს საკმარის არსებით ამინომჟავებს, შეგიძლიათ შეუთავსოთ ისინი პარკოსნებს და მიიღოთ საკმარისი ცილა და საკვები ნივთიერებები.
რა ცილებით მდიდარ საკვებს ანიჭებთ უპირატესობას?
ახალი ცოდნის ფორმირება. სალექციო ბლოკი.
თემის სასწავლო გეგმა:
1. ცილების როლი ორგანიზმში, ცილების ბუნებრივი წყაროები.
2.ცილების შემადგენლობა და სტრუქტურა.
3. ცილების ფუნქციები.
4. ცილების ფიზიკური და ქიმიური თვისებები.
5. ცილის სინთეზი.
6. ცილების ტრანსფორმაციები ორგანიზმში
ცოცხალ უჯრედში შემავალი ორგანული ნივთიერებებიდან ყველაზე მნიშვნელოვან როლს ცილები ასრულებენ. ისინი შეადგენენ უჯრედის მასის დაახლოებით 50%-ს. ცილების წყალობით ორგანიზმმა შეიძინა მოძრაობის, გამრავლების, ზრდის, საკვების შთანთქმის, გარე ზემოქმედებაზე რეაგირების უნარი და ა.შ.
"სიცოცხლე არის ცილოვანი სხეულების არსებობის გზა, რომლის არსებითი წერტილი არის ნივთიერებების მუდმივი გაცვლა მათ გარშემო არსებულ გარე ბუნებასთან და ამ მეტაბოლიზმის შეწყვეტასთან ერთად წყდება სიცოცხლეც, რაც იწვევს ცილის დაშლას." ენგელსი თავის ნაწერებში წერდა.
ცილები საკვები პროდუქტების აუცილებელი კომპონენტებია და შედის მედიკამენტებში.
ცილა ადამიანის საკვების მნიშვნელოვანი კომპონენტია. დიეტური ცილების ძირითადი წყაროებია: ხორცი, რძე, მარცვლეულის პროდუქტები, პური, თევზი, ბოსტნეული. პროტეინის საჭიროება დამოკიდებულია ასაკზე, სქესზე და აქტივობის ტიპზე. ჯანმრთელი ადამიანის ორგანიზმში უნდა იყოს ბალანსი შემომავალი ცილების რაოდენობასა და გამოთავისუფლებულ დაშლის პროდუქტებს შორის. ცილის მეტაბოლიზმის შესაფასებლად დაინერგა ცილის ბალანსის კონცეფცია. ზრდასრულ ასაკში ჯანმრთელ ადამიანს აქვს აზოტის ბალანსი, ე.ი. საკვების ცილებიდან მიღებული აზოტის რაოდენობა უდრის გამოყოფილ აზოტის რაოდენობას. ახალგაზრდა, მზარდ სხეულში გროვდება ცილოვანი მასა, ამიტომ აზოტის ბალანსი დადებითი იქნება, ე.ი. მიღებული აზოტის რაოდენობა აღემატება ორგანიზმიდან ამოღებულ რაოდენობას. ხანდაზმულებში, ისევე როგორც ზოგიერთ დაავადებაში, შეინიშნება აზოტის უარყოფითი ბალანსი. აზოტის ხანგრძლივი უარყოფითი ბალანსი იწვევს ორგანიზმის სიკვდილს.
უნდა გვახსოვდეს, რომ ზოგიერთ ამინომჟავას სითბოს დამუშავებისა და პროდუქტების გრძელვადიანი შენახვის დროს შეუძლია წარმოქმნას ორგანიზმისთვის შეუნელებელი ნაერთები, ე.ი. გახდეს "მიუწვდომელი". ეს ამცირებს ცილის ღირებულებას.
ცხოველური და მცენარეული ცილები ორგანიზმში განსხვავებულად შეიწოვება. თუ რძის, რძის პროდუქტების, კვერცხის ცილები შეიწოვება 96%, ხორცი და თევზი - 93-95%, მაშინ პურის ცილები - 62-86%, ბოსტნეული - 80%, კარტოფილი და ზოგიერთი პარკოსანი - 70%. თუმცა, ამ პროდუქტების ნარევი შეიძლება ბიოლოგიურად უფრო სრულყოფილი იყოს.
ორგანიზმის მიერ ცილების შეწოვის ხარისხზე გავლენას ახდენს საკვების წარმოების ტექნოლოგია და მათი კულინარიული დამუშავება. საკვები პროდუქტების ზომიერი გაცხელებით, განსაკუთრებით მცენარეული წარმოშობის, ცილების მონელება ოდნავ იზრდება. ინტენსიური თერმული დამუშავებით, საჭმლის მონელება მცირდება.
ზრდასრული ადამიანის ყოველდღიური მოთხოვნილება სხვადასხვა ტიპის ცილაზე არის 1–1,5 გ 1 კგ წონაზე, ე.ი. დაახლოებით 85-100 გ ცხოველური ცილების წილი უნდა იყოს მთლიანი რაოდენობის დაახლოებით 55%.
2. ცილების სტრუქტურა.
ბევრ ორგანულ ნაერთს, რომლებიც ქმნიან უჯრედს, ხასიათდება დიდი მოლეკულური ზომებით. რა ჰქვია ამ მოლეკულებს? (მაკრომოლეკულები) ისინი ჩვეულებრივ შედგება მსგავსი სტრუქტურის დაბალი მოლეკულური ნაერთებისგან, რომლებიც ერთმანეთთან არის დაკავშირებული კოვალენტური ბმებით. მათი სტრუქტურა შეიძლება შევადაროთ ძაფზე მძივებს. რა ჰქვია ამ კომპონენტებს? (მონომერები). ისინი ქმნიან პოლიმერებს. პოლიმერების უმეტესობა აგებულია ერთი და იგივე მონომერებისგან. ასეთ მონომერებს რეგულარულს უწოდებენ. მაგალითად, თუ A არის მონომერი, მაშინ –A-A-A-…….A არის პოლიმერი. პოლიმერებს, რომლებშიც მონომერები სტრუქტურით განსხვავებულია, არარეგულარული ეწოდება. მაგალითად, -A-V-R-P-A-……G-R-P-A-. შემადგენლობა განსაზღვრავს მათ თვისებებს.
ცილები არის არარეგულარული პოლიმერები, რომელთა მონომერები ამინომჟავებია.
ცილები არის რთული მაღალმოლეკულური ბუნებრივი ნაერთები, რომლებიც აგებულია ამინომჟავებისგან. პროტეინები შეიცავს 20 განსხვავებულ ამინომჟავას, რაც ნიშნავს, რომ არსებობს ცილების უზარმაზარი მრავალფეროვნება ამინომჟავების სხვადასხვა კომბინაციით. როგორც ანბანის 33 ასოდან უსასრულო რაოდენობის სიტყვის ფორმირება შეგვიძლია, 20 ამინომჟავისგან შეგვიძლია უსასრულო რაოდენობის ცილა. ადამიანის ორგანიზმში 100000-მდე ცილაა.
ცილების უმეტესობა შეიცავს 300-500 ამინომჟავის ნარჩენებს, მაგრამ ასევე არის უფრო დიდი ცილები, რომლებიც შედგება 1500 ან მეტი ამინომჟავისგან. ცილები განსხვავდებიან ამინომჟავების შემადგენლობით და ამინომჟავების ერთეულების რაოდენობით და განსაკუთრებით პოლიპეპტიდურ ჯაჭვებში მათი მონაცვლეობის თანმიმდევრობით. გამოთვლები აჩვენებს, რომ 20 სხვადასხვა ამინომჟავისგან აგებული ცილისთვის, რომელიც შეიცავს 100 ამინომჟავის ნარჩენებს ჯაჭვში, შესაძლო ვარიანტების რაოდენობა შეიძლება იყოს 10130.
ინსულინი -5700
რიბონუკლეაზა –12700
ალბუმინი-36000
ჰემოგლობინი-65000
ასეთი მასით ცილები გრძელი ძაფებით უნდა იყოს. მაგრამ მათ მაკრომოლეკულებს აქვთ კომპაქტური ბურთულების (გლობულების) ან წაგრძელებული სტრუქტურების (ბოჭკოვანი) ფორმულა.
პროტეინები იყოფა ცილებად (მარტივი ცილები) და პროტეიდებად (კომპლექსური ცილები). მოლეკულებში შემავალი ამინომჟავების ნარჩენების რაოდენობა განსხვავებულია, მაგალითად: ინსულინი - 51, მიოგლობინი - 140. აქედან გამომდინარე, Mr ცილა 10000-დან რამდენიმე მილიონამდეა.
პირველი ჰიპოთეზა ცილის მოლეკულის სტრუქტურის შესახებ შემოთავაზებული იქნა XIX საუკუნის 70-იან წლებში. ეს იყო ცილის სტრუქტურის ureide თეორია. 1903 წელს გერმანელმა მეცნიერმა ე.გ. ფიშერმა შემოგვთავაზა პეპტიდის თეორია, რომელიც გახდა ცილის სტრუქტურის საიდუმლოების გასაღები. ფიშერმა შესთავაზა, რომ ცილები არის ამინომჟავების ნარჩენების პოლიმერები, რომლებიც დაკავშირებულია NH–CO პეპტიდურ ბმასთან. მოსაზრება, რომ ცილები პოლიმერული წარმონაქმნებია, ჯერ კიდევ 1888 წელს გამოთქვა რუსმა მეცნიერმა A.Ya. ეს თეორია დადასტურდა შემდგომ ნაშრომებში. პოლიპეპტიდური თეორიის მიხედვით, ცილებს აქვთ სპეციფიკური სტრუქტურა
ბევრი ცილა შედგება რამდენიმე პოლიპეპტიდური ნაწილაკისგან, რომლებიც იკეცება ერთ აგრეგატში. ამრიგად, ჰემოგლობინის მოლეკულა (C738H1166S2Fe4O208) შედგება ოთხი ქვედანაყოფისგან. გაითვალისწინეთ, რომ ბატონი კვერცხის ცილა = 36,000, Mr კუნთის ცილა = 1,500,000.
პირველადი ცილის სტრუქტურა– ამინომჟავების ნარჩენების მონაცვლეობის თანმიმდევრობა ხორციელდება პეპტიდური (ამიდური) ბმების გამო, ყველა ბმა კოვალენტური და ძლიერია.
მეორადი სტრუქტურა- პოლიპეპტიდური ჯაჭვის ფორმა სივრცეში. ცილის ჯაჭვი ხვეულია სპირალურად, რომელიც ხორციელდება მრავალი წყალბადის ბმის გამო.
მესამეული სტრუქტურა– რეალური სამგანზომილებიანი კონფიგურაცია, რომელსაც გრეხილი სპირალი იღებს სივრცეში – პოლიპეპტიდური სპირალის ხვეული. (ელასტიური ტვინის ბურთის დემონსტრირება).
კონფიგურაციის წარმოდგენა ადვილია, მაგრამ უფრო რთულია იმის გაგება, თუ რა ძალები უჭერენ მხარს მას. (წყალბადის ბმები, დისულფიდური ხიდები -S-S-, ეთერული ბმები რადიკალებს შორის. პოლარული ჯგუფები COOH და OH ურთიერთქმედებენ წყალთან, ხოლო არაპოლარული რადიკალები აცილებენ მას, ისინი მიმართულია გლობულებში. რადიკალები ურთიერთქმედებენ ერთმანეთთან ვან დერ ვაალის ძალების გამო. .) (ჰიდროფობიური ბმების გამო), ზოგიერთ ცილაში - S–S ბმები (ბისულფიდური ხიდები), ესტერული ხიდები..
მეოთხეული სტრუქტურა- ერთმანეთთან დაკავშირებული ცილის მაკრომოლეკულები ქმნიან კომპლექსს. მეოთხეული სტრუქტურა - რამდენიმე პოლიპეპტიდური ჯაჭვის სტრუქტურა
შეიძლება სასარგებლო იყოს წაკითხვა:
- ინგლისური ფრაზები There is და There are;
- რა ჰქვია სარკეში ანარეკლს?;
- ბუნებრივი ცილების თვისებები;
- თეოდორე, ვოლგოგრადისა და კამიშინის მიტროპოლიტი (კაზანოვი ნიკოლაი ლვოვიჩი) როგორ მსახურობდა ეპისკოპოსი საავადმყოფოდან გაწერის შემდეგ;
- პეჩერსკის ხატმწერმა ალიპიუსმა, პატივცემულმა ხატმწერმა უნდა ამოიღოს ქრისტიანობის სულისადმი მტრული საგნები.;
- ძლიერი და სუსტი ზმნები: მოქმედების ინსტრუქციები;
- ძლიერი ზმნები გერმანულში;
- გერმანულში საქმეები მარტივია;